元素周期律是学习和研究化学的重要工具.下表是元素周期表的部分信息:
认真分析信息,回答:
(1)地壳中含量最多的金属元素的符号是 ;
(2) 表示的是(填符号) ;
表示的是(填符号) ;
(3)由7、8、12号元素组成化合物的化学式 ;
(4)上表中每一周期元素原子的变化规律是 .
| 1 H 氢 | 2 He 氦 | |||||||
| 3 Li 锂 | 4 Be 铍 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 | |
| 11 Na 钠 | 12 Mg 镁 | 13 Al 铝 | 14 Si 硅 | 15 P 磷 | 16 S 硫 | 17 Cl 氯 | 18 Ar 氩 | |
| 19 K 钾 | 20 Ga 钙 | … | ||||||
(1)地壳中含量最多的金属元素的符号是 ;
(2)
 表示的是(填符号) ;
表示的是(填符号) ;(3)由7、8、12号元素组成化合物的化学式 ;
(4)上表中每一周期元素原子的变化规律是 .
下表列出了1-18号元素的原子序数和元素符号:
请回答下列问题:
(1)l~18号元素中属于稀有气体元素的有He、Ne、 (填元素符号).
(2)l~18号元素中最外层有2个电子的原子有 、Be、Mg(填元素符号).
(3)某元素的原子结构示意图为 ,它在化学反应中一般易 电子(填“得到”
,它在化学反应中一般易 电子(填“得到”
或“失去”),它与地壳中含量最多的金属元素形成化合物的化学式为 .
(4)某粒子的结构示意图为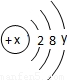 ,当x-y=8时,该粒子为 .
,当x-y=8时,该粒子为 .
(5)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质.下列各组粒子中属于等电子体的是 (填序号字母).
A、NO和O2B、CO和N2C、SO2和CO2D、PO43-和SO42-.
| 原子序数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 元素符号 | H | He | Li | Be | B | C | N | O | F |
| 原子序数 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 元素符号 | Ne | Na | Mg | Al | Si | P | S | Cl | Ar |
(1)l~18号元素中属于稀有气体元素的有He、Ne、 (填元素符号).
(2)l~18号元素中最外层有2个电子的原子有 、Be、Mg(填元素符号).
(3)某元素的原子结构示意图为
 ,它在化学反应中一般易 电子(填“得到”
,它在化学反应中一般易 电子(填“得到”或“失去”),它与地壳中含量最多的金属元素形成化合物的化学式为 .
(4)某粒子的结构示意图为
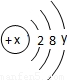 ,当x-y=8时,该粒子为 .
,当x-y=8时,该粒子为 .(5)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质.下列各组粒子中属于等电子体的是 (填序号字母).
A、NO和O2B、CO和N2C、SO2和CO2D、PO43-和SO42-.
己知电子的质量约为质子(或中子)质量的 ,下表是几种原子的组成和它们的相对原子质量.
,下表是几种原子的组成和它们的相对原子质量.
通过此表可总结出如“同一原子中质子数=核外电子数”等结论,请你再总结出两条规律:
① ;
② ;
③ .
0 78105 78113 78119 78123 78129 78131 78135 78141 78143 78149 78155 78159 78161 78165 78171 78173 78179 78183 78185 78189 78191 78195 78197 78199 78200 78201 78203 78204 78205 78207 78209 78213 78215 78219 78221 78225 78231 78233 78239 78243 78245 78249 78255 78261 78263 78269 78273 78275 78281 78285 78291 78299 211419
 ,下表是几种原子的组成和它们的相对原子质量.
,下表是几种原子的组成和它们的相对原子质量.| 原子种类 | 原子核 | 核外电子数 | 相对原子质量 | |
| 质子数 | 中子数 | |||
| 氢(H) | 1 | 1 | 1 | |
| 氦(He) | 2 | 2 | 2 | 4 |
| 氮(N) | 7 | 7 | 7 | 14 |
| 氧(O) | 8 | 8 | 8 | 16 |
| 铁(Fe) | 26 | 30 | 26 | 56 |
| 铀235(U235) | 92 | 143 | 92 | 235 |
① ;
② ;
③ .
 (1)(现在使用的氮肥大多是尿素[CO(NH2)2]和碳酸氢铵[NH4HCO3],请通过计算比较一下两种氮肥的含氮量的大小.
(1)(现在使用的氮肥大多是尿素[CO(NH2)2]和碳酸氢铵[NH4HCO3],请通过计算比较一下两种氮肥的含氮量的大小.


