石灰石是工业上的一种重要原料,其主要成分是碳酸钙.小黄为了测定从某矿山采来的石灰石中碳酸钙的质量分数,将样品与稀盐酸放在烧杯中反应进行实验,测定的有关实验数据如下表(石灰石中的杂质不参加反应):
| 实验次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| 加入的盐酸的质量/g | 50.00 | 50.00 | 50.00 | 50.00 |
| 石灰石样品的质量/g | 5.00 | 10.00 | 15.00 | 20.00 |
| 通过计算,生成的二氧化碳的质量/g | 1.76 | 3.52 | 4.40 | 4.40 |
(1)要计算出生成的二氧化碳的质量,还需要测定反应后烧杯中所有剩余物质的质量,请指出在第三次实验中,测定的烧杯中所有剩余物质的质量为________g;
(2)哪几次实验的反应中反应物有剩余?________;
(3)这种石灰石中碳酸钙的质量分数为________.
 水与人类的生活和生产密切相关.请回答下列问题.
水与人类的生活和生产密切相关.请回答下列问题.
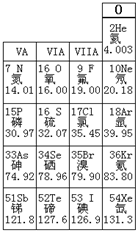 表是元素周期表的一部分,请回答:
表是元素周期表的一部分,请回答: