实验室可用KClO3和MnO2的固体混合物加热制取氧气.现取30.5g的固体混合物加热一段时间收集到一定质量的氧气后,停止反应.
(1)欲求得氧气的质量,将试管中的剩余物冷却到室温后,通过向该试管分多次加水测定剩余物质的办法求得.加水的质量与剩余固体的质量见下表:(MnO2不溶于水)
表中m的值为 ,所得氧气的质量为 .
(2)为了测定固体混合物中MnO2的质量分数,需用 方法回收MnO2.
实验结束后,有3位同学分别展示了所测MnO2的质量分数.
老师的评价是:小东结果偏高,小南、小西结果偏低.于是全班同学讨论误差,下列所找原因正确的是(填序号) .
①小东:称量KClO3和MnO2固体混合物时将固体放在天平的右边(1g以下用砝码)
②小东:滤液浑浊就干燥
③小东:烧杯里的物质还未充分溶解就开始过滤
④小南:称余下固体时只在天平的左盘垫了张纸
⑤小西:称余下固体前,部分固体洒落地下
(3)若要证明MnO2是该反应的催化剂,还需补做两个实验:①证明MnO2在反应前后化学性质不变.
②证明MnO2能改变KClO3反应放出氧气的速率.完成②需选用下图装置中的(填序号) .要比较产生O2的快慢,除可以直接观察气泡产生的快慢,还可以 .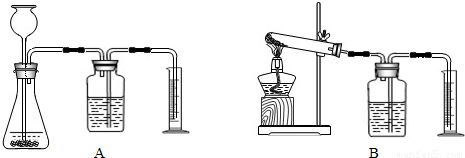
(1)欲求得氧气的质量,将试管中的剩余物冷却到室温后,通过向该试管分多次加水测定剩余物质的办法求得.加水的质量与剩余固体的质量见下表:(MnO2不溶于水)
| 编号 | 1 | 2 | 3 | 4 |
| 加水的质量(g) | 20 | 20 | 20 | 20 |
| 剩余固体的质量(g) | 14.5 | 8.1 | m | 6 |
(2)为了测定固体混合物中MnO2的质量分数,需用 方法回收MnO2.
实验结束后,有3位同学分别展示了所测MnO2的质量分数.
| 小东 | 小南 | 小西 | |
| MnO2% | 35% | 10% | 15% |
①小东:称量KClO3和MnO2固体混合物时将固体放在天平的右边(1g以下用砝码)
②小东:滤液浑浊就干燥
③小东:烧杯里的物质还未充分溶解就开始过滤
④小南:称余下固体时只在天平的左盘垫了张纸
⑤小西:称余下固体前,部分固体洒落地下
(3)若要证明MnO2是该反应的催化剂,还需补做两个实验:①证明MnO2在反应前后化学性质不变.
②证明MnO2能改变KClO3反应放出氧气的速率.完成②需选用下图装置中的(填序号) .要比较产生O2的快慢,除可以直接观察气泡产生的快慢,还可以 .

填写“探究微粒运动”的实验报
0 77335 77343 77349 77353 77359 77361 77365 77371 77373 77379 77385 77389 77391 77395 77401 77403 77409 77413 77415 77419 77421 77425 77427 77429 77430 77431 77433 77434 77435 77437 77439 77443 77445 77449 77451 77455 77461 77463 77469 77473 77475 77479 77485 77491 77493 77499 77503 77505 77511 77515 77521 77529 211419
| 实验步骤 | 现象 | 结论 |
| 在盛有少量水的试管里滴2至3滴无色酚酞试液 | 无色酚酞____(变色、不变色). | 水_____使无色酚酞试液变色. |
| 在试管里盛少量的浓氨水,小心闻氨水的气味,再在盛有氨水的试管里滴2至3滴无色酚酞试液. | 浓氨水_____气味, 无色酚酞试液_____. | 浓氨水容易_____,氨水_____使酚酞试液变红色. |
| 在小烧杯A中加入20ml的蒸馏水,并滴入2至3滴酚酞.在小烧杯B中加入3ml至5ml的浓氨水,再用一只大烧杯将A、B两烧杯罩在一起. | A烧杯中的溶液_____,B烧杯中的溶液_____. |

