某化学实验小组在探究物质燃烧条件时,用一个集气瓶罩住燃着的小蜡烛,小蜡烛一会儿就熄灭了.它为什么会熄灭呢?每个人都提出了不同的猜想.
[猜想]甲同学猜想:蜡烛燃烧耗尽了瓶内的氧气,所以它熄灭了;
乙同学猜想:蜡烛燃烧后,瓶内二氧化碳的浓度过高导致了蜡烛熄灭;
丙同学猜想:甲、乙两位同学都只看到了问题的一个方面,他认为两人的猜想都有道理;
丁同学猜想:______.
[查阅资料]①白磷的着火点是40℃;②生石灰(CaO)与水发生化学
反应:CaO+H2OCa(OH)2,同时放出大量的热.
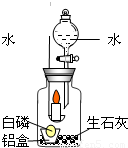
[实验设计]大家激烈地讨论,很难达成一致.于是丁同学设计了如右图所示的装置来验证自己的猜想.
2P2O5
[猜想]甲同学猜想:蜡烛燃烧耗尽了瓶内的氧气,所以它熄灭了;
乙同学猜想:蜡烛燃烧后,瓶内二氧化碳的浓度过高导致了蜡烛熄灭;
丙同学猜想:甲、乙两位同学都只看到了问题的一个方面,他认为两人的猜想都有道理;
丁同学猜想:______.
[查阅资料]①白磷的着火点是40℃;②生石灰(CaO)与水发生化学
反应:CaO+H2OCa(OH)2,同时放出大量的热.
[实验设计]大家激烈地讨论,很难达成一致.于是丁同学设计了如右图所示的装置来验证自己的猜想.
| 实验步骤 | 实验现象 | 实验分析 | 实验结论 |
| 1.取一小块白磷放在一铝箔制的小盒中,然后放入装有生石灰的集气瓶内,点燃蜡烛,塞紧胶塞,观察现象. | 燃烧的蜡烛一会儿就熄灭了. | 蜡烛燃烧需满足的条件: ①温度达到着火点 ②______ | 丁同学的猜想是正确的 |
| 2.待冷却后,打开分液漏斗活塞,向集气瓶中注入少量的水,立即关闭活塞,观察现象. | 铝盒中的白磷燃烧,放出热量的同时产生了白烟. | 白磷燃烧满足的条件与蜡烛燃烧的条件相同,白磷燃烧的方程式:______ |

某药厂生产的葡萄糖酸锌口服液的标签如右图所示,请回答下列问题:
(1)葡萄糖酸锌是由______种元素组成;其氢、氧元素的质量比为______.
(2)每支口服液含葡萄糖酸锌45.5mg,请你计算标签中每支口服液含锌元素的质量为______mg.
| ××牌口服液 主要成分:葡萄糖酸锌 化学式:C12H22O14Zn 含锌量:每支口服液含锌 mg ××制药厂 |
(2)每支口服液含葡萄糖酸锌45.5mg,请你计算标签中每支口服液含锌元素的质量为______mg.
我县西田各庄镇西智地区山上含有大量石灰石(主要成分为碳酸钙),为测定石灰石中碳酸钙的含量,某学校课外小组同学做了如下实验:首先称取50g该地区的石灰石样品,然后将150mL的稀盐酸分5次加入(假设其余杂质均不与盐酸反应)进行充分反应.实验过程中的数据记录如下
(1)X=______g;
(2)计算该石灰石样品中碳酸钙的质量分数是多少?
(3)若把该反应产生的二氧化碳全部收集起来,共有多少L?
(注意:①二氧化碳气体的密度为1.977g/L,②要求写出全部计算过程)
0 77204 77212 77218 77222 77228 77230 77234 77240 77242 77248 77254 77258 77260 77264 77270 77272 77278 77282 77284 77288 77290 77294 77296 77298 77299 77300 77302 77303 77304 77306 77308 77312 77314 77318 77320 77324 77330 77332 77338 77342 77344 77348 77354 77360 77362 77368 77372 77374 77380 77384 77390 77398 211419
| 稀盐酸的体积 | 第一次30mL | 第二次30mL | 第三次30mL | 第四次30mL | 第五次30mL |
| 剩余固体质量 | 40.0g | X | 20.0g | 10.0g | 5.0g |
(2)计算该石灰石样品中碳酸钙的质量分数是多少?
(3)若把该反应产生的二氧化碳全部收集起来,共有多少L?
(注意:①二氧化碳气体的密度为1.977g/L,②要求写出全部计算过程)
 沉降→过滤→吸附
沉降→过滤→吸附 自来水,其中常用的消毒剂是( )
自来水,其中常用的消毒剂是( )