物质丙是重要的化工产品,在国民经济中占有重要地位.工业上用甲和乙合成丙.甲、乙、丙的微观示意图见下表.
(1)甲、乙、丙三种物质都是由(填“分子”、“原子”或“离子”) 构成的.
(2)甲、乙、丙中属于化合物的是(填序号) .
(3)已知物质丙中氢元素的化合价为+1,则另一种元素的化合价为 .
(4)甲和乙合成丙的反应中,甲、乙、丙的微粒个数比为 .
(5)现有10g 的甲和60g 的乙混合反应制取丙,反应一段时间后,经测定剩余甲的质量为4g,则剩余乙的质量为 g.
| 物质 | 甲 | 乙 | 丙 |   |
| 微观示意图 |  |  |  |
(2)甲、乙、丙中属于化合物的是(填序号) .
(3)已知物质丙中氢元素的化合价为+1,则另一种元素的化合价为 .
(4)甲和乙合成丙的反应中,甲、乙、丙的微粒个数比为 .
(5)现有10g 的甲和60g 的乙混合反应制取丙,反应一段时间后,经测定剩余甲的质量为4g,则剩余乙的质量为 g.
某实验小组探究火锅烟气中CO2、CO分别对人体血液供氧能力的影响.设计装置如图所示(试管中均为稀释的新鲜鸡血):
实验记录:
(1)向试管①中通入气体时,气体从导管口(填装置图中的序号)______处通入.
(2)试管②的作用是______.
(3)气体A为______.判断的依据是______.
(4)从安全和环保的角度来看,本实验需要改进的地方是______.
(5)通过实验可以得出结论,火锅烟气中对人体血液供氧量有影响的是(填具体物质)______.

实验记录:
| 操作步骤 | 现象 | |
| I. | 分别向试管①、②、③中通入氧气 | 鸡血颜色为鲜红色 |
| II. | 向试管①中通入气体A; 停止通入A,向试管①中通入氧气 | 鸡血颜色由鲜红色变为桃红色 鸡血颜色不变 |
| III. | 向试管③中通入气体B; 停止通入B,向试管③中通入氧气 | 鸡血颜色由鲜红色变为暗红色 鸡血颜色由暗红色变为鲜红色 |
(2)试管②的作用是______.
(3)气体A为______.判断的依据是______.
(4)从安全和环保的角度来看,本实验需要改进的地方是______.
(5)通过实验可以得出结论,火锅烟气中对人体血液供氧量有影响的是(填具体物质)______.

碳酸钙可用于预防和治疗钙缺乏症.某实验小组同学要测定一种钙片中碳酸钙的含量.
查阅资料:获得的资料有:
(1)补钙剂中常加入糖类、维生素D等改善口感或增强药效.这些物质不与稀盐酸反应产生气体,高温灼烧时会燃烧或分解.
(2)碳酸钙高温灼烧分解生成氧化钙和二氧化碳.
(3)常见的碳酸钙含量测定方法:将碳酸钙粉碎,加入已知浓度的过量盐酸充分反应,然后测剩余盐酸的量,根据消耗盐酸的量最终求得碳酸钙的含量.
(4)澄清石灰水中的Ca(OH)2含量很少,100g澄清石灰水中最多含0.15g Ca(OH)2.
方案设计和实施:根据资料和已学知识,该小组同学设计如下两种方案进行测定.
方案1:根据下图所示装置实验.
(1)锥形瓶中发生反应的化学方程式为______.
(2)长颈漏斗下部插入液面下的目的是______.
(3)加入药品前,检验该装置气密性的方法是______.
(4)记录数据如下:
方案2:将钙片粉碎,加入足量的稀盐酸充分反应,根据放出气体的量计算碳酸钙的含量.记录数据如下(空烧杯质量为100g,加入钙片质量为25g):
分析和评价:
(1)方案1和方案2中合理的是______,原因是______.
(2)该小组同学没有使用碳酸钙高温灼烧分解的方法(实验室可以进行该实验),原因是______.
(3)要使用查阅资料(3)中介绍的方法,还需要学习的是______.
结论:经过计算,该钙片中碳酸钙的质量分数是______.

0 75730 75738 75744 75748 75754 75756 75760 75766 75768 75774 75780 75784 75786 75790 75796 75798 75804 75808 75810 75814 75816 75820 75822 75824 75825 75826 75828 75829 75830 75832 75834 75838 75840 75844 75846 75850 75856 75858 75864 75868 75870 75874 75880 75886 75888 75894 75898 75900 75906 75910 75916 75924 211419
查阅资料:获得的资料有:
(1)补钙剂中常加入糖类、维生素D等改善口感或增强药效.这些物质不与稀盐酸反应产生气体,高温灼烧时会燃烧或分解.
(2)碳酸钙高温灼烧分解生成氧化钙和二氧化碳.
(3)常见的碳酸钙含量测定方法:将碳酸钙粉碎,加入已知浓度的过量盐酸充分反应,然后测剩余盐酸的量,根据消耗盐酸的量最终求得碳酸钙的含量.
(4)澄清石灰水中的Ca(OH)2含量很少,100g澄清石灰水中最多含0.15g Ca(OH)2.
方案设计和实施:根据资料和已学知识,该小组同学设计如下两种方案进行测定.
方案1:根据下图所示装置实验.
(1)锥形瓶中发生反应的化学方程式为______.
(2)长颈漏斗下部插入液面下的目的是______.
(3)加入药品前,检验该装置气密性的方法是______.
(4)记录数据如下:
| 钙片质量 | 空洗气瓶质量 | 澄清石灰水的质量 | 反应后洗气瓶及瓶内物质总质量 |
| 25g | 100g | 200g | 300.4g |
| 加入稀盐酸的质量 | 100g | 200g | 300g | 400g |
| 充分反应后烧杯及杯内物质总质量 | 222.8g | 320.6g | 418.4g | 518.4g |
(1)方案1和方案2中合理的是______,原因是______.
(2)该小组同学没有使用碳酸钙高温灼烧分解的方法(实验室可以进行该实验),原因是______.
(3)要使用查阅资料(3)中介绍的方法,还需要学习的是______.
结论:经过计算,该钙片中碳酸钙的质量分数是______.




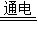 4Al+3O2↑.如果加工一个铝锅需要1.08Kg的铝,至少需要电解多少质量的氧化铝才能制成这个铝锅?
4Al+3O2↑.如果加工一个铝锅需要1.08Kg的铝,至少需要电解多少质量的氧化铝才能制成这个铝锅?