某化学课外兴趣小组探究氢气还原氧化铜的反应,有如下实验装置:
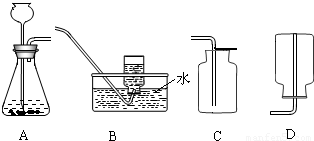
(1)上述A装置可用于实验室制取氢气和二氧化碳,请分别写出实验室制取氢气和二氧化碳
的化学方程式______;______;
上述可用于收集二氧化碳装置是______(用装置字母序号填空).
(2)请你参与探究氢气还原氧化铜得到的红色固体的成分,完成下列各题:
已知信息:Ⅰ.氢气还原氧化铜除生成铜外还可能生成氧化亚铜(Cu2O);Ⅱ.Cu和Cu2O均为不溶于水的红色固体;Ⅲ.Cu2O+H2SO4=CuSO4+Cu+H2O
提出问题:红色固体含有什么物质?
①猜想假设:
假设一:红色固体只含Cu;假设二:红色固体只含Cu2O;
假设三:______(请补充完成假设三).
②实验探究:(填写表中空格)
③数据处理:甲同学称取Wg红色固体加入到足量硫酸溶液中使其充分反应后,______(填操作名称)、洗涤、干燥,称量剩余红色固体质量为mg,通过计算,若m______ 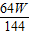 g(选填>、<或=),则假设二成立;若m______
g(选填>、<或=),则假设二成立;若m______ 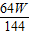 g(选填>、<或=),则假设三成立.
g(选填>、<或=),则假设三成立.
④交流与反思:只要假设合理,实验方法正确,根据实验现象和数据就能得出结论.

(1)上述A装置可用于实验室制取氢气和二氧化碳,请分别写出实验室制取氢气和二氧化碳
的化学方程式______;______;
上述可用于收集二氧化碳装置是______(用装置字母序号填空).
(2)请你参与探究氢气还原氧化铜得到的红色固体的成分,完成下列各题:
已知信息:Ⅰ.氢气还原氧化铜除生成铜外还可能生成氧化亚铜(Cu2O);Ⅱ.Cu和Cu2O均为不溶于水的红色固体;Ⅲ.Cu2O+H2SO4=CuSO4+Cu+H2O
提出问题:红色固体含有什么物质?
①猜想假设:
假设一:红色固体只含Cu;假设二:红色固体只含Cu2O;
假设三:______(请补充完成假设三).
②实验探究:(填写表中空格)
| 实验操作 | 实验现象 | 实验结论 |
| a.取少量红色固体加入到足量硫酸溶液中 | 无明显现象 | 假设______成立 |
| b.取少量红色固体加入到足量硫酸溶液中 | ______ | 假设二和假设三均成立 |
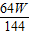 g(选填>、<或=),则假设二成立;若m______
g(选填>、<或=),则假设二成立;若m______ 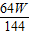 g(选填>、<或=),则假设三成立.
g(选填>、<或=),则假设三成立.④交流与反思:只要假设合理,实验方法正确,根据实验现象和数据就能得出结论.
某兴趣小组购得用于食用菌种植的轻质碳酸钙(杂质不与盐酸反应,也不含钙元素),标签如左下图.为了测定其含钙量,该小组.利用电子天平测定的有关实验数据如下表:
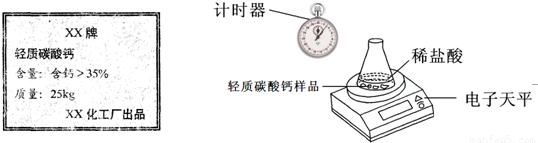
试求:
(1)反应产生的二氧化碳气体的质量.
(2)样品中碳酸钙的质量分数.
(3)通过计算说明标签标示的含钙量是否正确.

| 称量项目 | 质量/g |
| 轻质碳酸钙样品 | 10.00 |
| 锥形瓶 | 100.00 |
| 锥形瓶+稀盐酸(足量) | 139.20 |
| 锥形瓶+稀盐酸+固体混合物(反应开始15秒) | 145.60 |
| 锥形瓶+稀盐酸+固体混合物(反应开始35秒) | 145.24 |
| 锥形瓶+稀盐酸+固体混合物(反应开始55秒) | 145.20 |
(1)反应产生的二氧化碳气体的质量.
(2)样品中碳酸钙的质量分数.
(3)通过计算说明标签标示的含钙量是否正确.
在一个密闭容器中有四种物质,在一定条件下充分反应后,测得反应前后各物质的质量如下:
已知x的相对分子质量为n,Q的相对分子质量为2n,则下列推断正确的是( )
A.反应后Q的质量为10g
B.反应中Y与Q发生改变的质量比为1:1
C.反应后生成15gZ
D.该反应方程式中X与Q的化学计量数之比为2:3
0 75109 75117 75123 75127 75133 75135 75139 75145 75147 75153 75159 75163 75165 75169 75175 75177 75183 75187 75189 75193 75195 75199 75201 75203 75204 75205 75207 75208 75209 75211 75213 75217 75219 75223 75225 75229 75235 75237 75243 75247 75249 75253 75259 75265 75267 75273 75277 75279 75285 75289 75295 75303 211419
| 物 质 | X | Y | Z | Q |
| 反应前质量/g | 4 | 10 | 1 | 21 |
| 反应后质量/g | 12 | 15 | 待测 |
A.反应后Q的质量为10g
B.反应中Y与Q发生改变的质量比为1:1
C.反应后生成15gZ
D.该反应方程式中X与Q的化学计量数之比为2:3




 4CO2+2X+6H2O.下列叙述不正确的是( )
4CO2+2X+6H2O.下列叙述不正确的是( )



