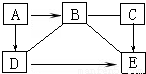
为除去物质中的杂质(括号内为杂质),所选用试剂和操作方法都正确的是( )
A.A
B.B
C.C
D.D
| 物 质 | 选用试剂 | 操作方法 | |
| A | CO2(HCl) | NaOH溶液 | 加入过量NaOH溶液 |
| B | Cu(Fe) | CuSO4溶液 | 加入过量CuSO4溶液,充分反应后过滤 |
| C | KCl(MnO2) | 水 | 加水溶解,然后过滤、洗涤、干燥 |
| D | CaCl2(HCl)溶液 | 碳酸钙 | 加入过量碳酸钙,充分反应后过滤 |
A.A
B.B
C.C
D.D
向下表的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成气体或沉淀的质量与加入乙的质量关系,能用如图所示曲线表示的是( )

A.A
B.B
C.C
D.D
| 序号 | 甲 | 乙 |
| A | 铜、锌的混合物 | 稀盐酸 |
| B | 硫酸和硫酸铜的混合溶液 | 氢氧化钠溶液 |
| C | 盐酸和硫酸的混合溶液 | 氯化钡溶液 |
| D | 铁钉 | 稀盐酸 |

A.A
B.B
C.C
D.D
小军用如图形式对所学知识进行归纳,其中甲包含乙、丙、丁…,根据示例,完成①②③例中甲栏或“乙、丙、丁”栏的填空,其中“乙、丙、丁”栏中不足三种物质的要补足三种,第③例任意列举,但需前后对应,各例甲栏内容均不能重复.

| 甲 | 乙、丙、丁 | |
| 示例 | 盐 | 食盐、纯碱、高锰酸钾 |
| ① | 营养物质 | 蛋白质、糖类、______ |
| 质子、中子、电子 | ||
| ③ |

某学生在A、B、C、D四个平底烧瓶中分别放入干燥的铁钉、一半浸在食盐水的铁钉、一半浸在蒸馏水的铁钉、完全浸没在蒸馏水中的铁钉,然后装配成如图所示的四套装置中,每隔一段时间测量导管中水面的高度,结果如表所示(表中所列数据都为导管水面上升的高度/cm,导管大小完全相同).
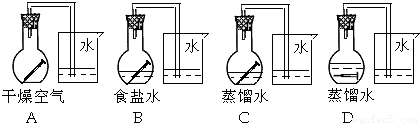
请回答下列问题:
(1)导管中水面为什么会上升?______.
(2)上述实验中,铁生锈的速率由大到小的顺序为(填烧瓶代号)______.
(3)实验表明,影响铁生锈的因素有______.

| 时间/小时 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | |
| A瓶(盛干燥铁钉) | |||||||
| B瓶(盛半浸在食盐水的铁钉) | 0.4 | 1.2 | 3.4 | 5.6 | 7.6 | 9.8 | |
| C瓶(盛半浸在蒸馏水的铁钉) | 0.3 | 0.8 | 2.0 | 3.5 | |||
| D瓶(铁钉完全浸没在蒸馏水中) |
(1)导管中水面为什么会上升?______.
(2)上述实验中,铁生锈的速率由大到小的顺序为(填烧瓶代号)______.
(3)实验表明,影响铁生锈的因素有______.
下载:
某化学兴趣小组有一次活动的内容是:对一包铁矿石粉末的组成进行探究,请你参与并回答有关问题.
[教师提醒]它由菱铁矿(FeCO3)、赤铁矿(Fe2O3)、磁铁矿(Fe3O4)三种固体粉末中的一种或两种组成.
[提出猜想]试样粉末主要成分可能有:①只是FeCO3、②只是Fe2O3、③只是Fe3O4、④FeCO3和Fe2O3、⑤FeCO3和Fe3O4、⑥Fe2O3和Fe3O4.
[查阅资料](1)FeCO3受热易分解FeCO3 FeO+CO2↑,常温与可盐酸反应放出CO2:FeCO3+2HCl=FeCl2+CO2↑+H2O,
FeO+CO2↑,常温与可盐酸反应放出CO2:FeCO3+2HCl=FeCl2+CO2↑+H2O,
(2)铁矿石粉末中的杂质不参加反应.
[探究思路]先利用物质的性质不同设计实验探究其成分,然后再选择适当的试剂和方法通过实验测定其含量.(装置内空气中的水蒸气、CO2忽略不计)
[实验探究]
(1)取适量试样粉末装入试管中,加入适量的盐酸,没有气泡产生,从而排除猜想中的______(填猜想中的序号).
(2)为进一步确定试样粉末的组成,称取该粉末10.0g装入硬质玻璃管中,在通风厨按如图进行实验.

开始时缓缓通入CO气体,过一段时间后再加热使其充分反应.待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却.反应前后称量相关装置和物质的总质量,其数据如下表:
[交流讨论]
(3)为了防止溶液倒吸,本实验最后停止加热前是否需要先断开装置中a和b的连接处?______(填需要或不需要),理由是______.
(4)b装置中可能会发生多个化学反应,任写出其中1个反应的化学方程式:______.
[反思评价]
(5)本实验的尾气是否需处理?如需处理,请回答如何处理,如不需处理,请说明理由:______.
(6)通过计算确定,该铁矿石试样的主要成分,指出哪个猜想是正确的(已知铁矿石的纯度为80.0%).
解:
0 72558 72566 72572 72576 72582 72584 72588 72594 72596 72602 72608 72612 72614 72618 72624 72626 72632 72636 72638 72642 72644 72648 72650 72652 72653 72654 72656 72657 72658 72660 72662 72666 72668 72672 72674 72678 72684 72686 72692 72696 72698 72702 72708 72714 72716 72722 72726 72728 72734 72738 72744 72752 211419
某化学兴趣小组有一次活动的内容是:对一包铁矿石粉末的组成进行探究,请你参与并回答有关问题.
[教师提醒]它由菱铁矿(FeCO3)、赤铁矿(Fe2O3)、磁铁矿(Fe3O4)三种固体粉末中的一种或两种组成.
[提出猜想]试样粉末主要成分可能有:①只是FeCO3、②只是Fe2O3、③只是Fe3O4、④FeCO3和Fe2O3、⑤FeCO3和Fe3O4、⑥Fe2O3和Fe3O4.
[查阅资料](1)FeCO3受热易分解FeCO3
 FeO+CO2↑,常温与可盐酸反应放出CO2:FeCO3+2HCl=FeCl2+CO2↑+H2O,
FeO+CO2↑,常温与可盐酸反应放出CO2:FeCO3+2HCl=FeCl2+CO2↑+H2O,(2)铁矿石粉末中的杂质不参加反应.
[探究思路]先利用物质的性质不同设计实验探究其成分,然后再选择适当的试剂和方法通过实验测定其含量.(装置内空气中的水蒸气、CO2忽略不计)
[实验探究]
(1)取适量试样粉末装入试管中,加入适量的盐酸,没有气泡产生,从而排除猜想中的______(填猜想中的序号).
(2)为进一步确定试样粉末的组成,称取该粉末10.0g装入硬质玻璃管中,在通风厨按如图进行实验.

开始时缓缓通入CO气体,过一段时间后再加热使其充分反应.待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却.反应前后称量相关装置和物质的总质量,其数据如下表:
| 反应前 | 反应后 | |
| a管 | 玻璃管和试样粉末的总质量为70.0g | 玻璃管和固体物质的总质量为67.6g |
| b瓶 | 洗气瓶和所盛溶液的总质量为200.0g | 洗气瓶和瓶中物质的总质量为206.6g |
(3)为了防止溶液倒吸,本实验最后停止加热前是否需要先断开装置中a和b的连接处?______(填需要或不需要),理由是______.
(4)b装置中可能会发生多个化学反应,任写出其中1个反应的化学方程式:______.
[反思评价]
(5)本实验的尾气是否需处理?如需处理,请回答如何处理,如不需处理,请说明理由:______.
(6)通过计算确定,该铁矿石试样的主要成分,指出哪个猜想是正确的(已知铁矿石的纯度为80.0%).
解: