石灰石是工业上的一种重要原料,其主要成分是碳酸钙.小黄为了测定从某矿山采来的石灰石中碳酸钙的质量分数,将样品与稀盐酸放在烧杯中反应进行实验,测定的有关实验数据如下表(石灰石中的杂质不参加反应):
(反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O)
(1)要计算出生成的二氧化碳的质量,还需要测定反应后烧杯中所有剩余物质的质量,请指出在第三次实验中,测定的烧杯中所有剩余物质的质量为 g;
(2)哪几次实验的反应中反应物有剩余? ;
(3)这种石灰石中碳酸钙的质量分数为 .
0 71149 71157 71163 71167 71173 71175 71179 71185 71187 71193 71199 71203 71205 71209 71215 71217 71223 71227 71229 71233 71235 71239 71241 71243 71244 71245 71247 71248 71249 71251 71253 71257 71259 71263 71265 71269 71275 71277 71283 71287 71289 71293 71299 71305 71307 71313 71317 71319 71325 71329 71335 71343 211419
| 实验次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| 加入的盐酸的质量/g | 50.00 | 50.00 | 50.00 | 50.00 |
| 石灰石样品的质量/g | 5.00 | 10.00 | 15.00 | 20.00 |
| 通过计算,生成的二氧化碳的质量/g | 1.76 | 3.52 | 4.40 | 4.40 |
(1)要计算出生成的二氧化碳的质量,还需要测定反应后烧杯中所有剩余物质的质量,请指出在第三次实验中,测定的烧杯中所有剩余物质的质量为 g;
(2)哪几次实验的反应中反应物有剩余? ;
(3)这种石灰石中碳酸钙的质量分数为 .


 F+H2O B+E
F+H2O B+E  F+G
F+G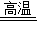 F+G D+C(不足)
F+G D+C(不足) B
B
