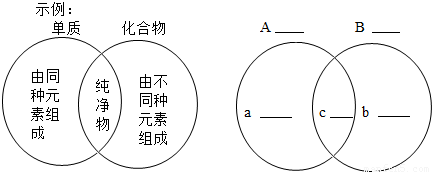
已知几种原子和离子的结构,带电情况以及化合价如下表:
通过此表可以总结出“带负电荷的原子属于阴离子”,还可以总结出:
(1)
(2)
(3) .
| 粒子结构 示意图 | 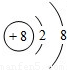 | 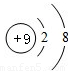 | 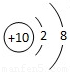 | 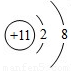 | 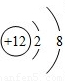 |
| 粒子类型 | 阴离子 | 阴离子 | 原子 | 阳离子 | 阳离子 |
| 粒子所带电荷 | 2个单位负电荷 | 1个单位负电荷 | 不显电性 | 1个单位正电荷 | 2个单位正电荷 |
| 化合价 | -2 | -1 | +1 | +2 |
(1)
(2)
(3) .
我们周围的物质世界是由100多种元素组成的,为了便于研究元素的性质,常常需要寻找它们之间的内在规律.下表列出的是1~18号元素的部分最高正化合价和最低负化合价.请你阅读后,回答下列问题:
(1)很多科学家对元素周期表的发现和完善做出了重大贡献,请写出其中一位科学家的名字______.
(2)表中不同种元素最本质的区别是______(填序号).
A.质子数不同 B.中子数不同
C.相对原子质量不同 D.电子数不同
(3)11号元素属于______元素(填“金属”或“非金属”),它在化学反应中形成的粒子与______(写元素符号)原子具有相同的核外电子排布.
(4)16号元素的原子核外电子数为______,推测该元素最低负化合价为______价,最高正化合价的氧化物的化学式为______.
(5)从化合价角度分析,我们可以发现一些规律.请写出其中的一个:______.
(6)某元素R与硫酸根形成化合物的化学式为:RSO4,其相对分子质量为152,回答下列问题:
①R的元素符号为______.
②R在化合物中可以显+3价,则+3价R的氧化物的化学式为______,+3价R的氧化物中R的质量分数是多少?(写出计算过程)
0 68477 68485 68491 68495 68501 68503 68507 68513 68515 68521 68527 68531 68533 68537 68543 68545 68551 68555 68557 68561 68563 68567 68569 68571 68572 68573 68575 68576 68577 68579 68581 68585 68587 68591 68593 68597 68603 68605 68611 68615 68617 68621 68627 68633 68635 68641 68645 68647 68653 68657 68663 68671 211419
| 1H +1 | 2He | ||||||
| 3Li +1 | 4Be +2 | 5B +3 | 6C +4,-4 | 7N +5,-3 | 8O -2 | 9F -1 | 10Ne |
| 11Na +1 | 12Mg +2 | 13Al +3 | 14Si +4,-4 | 15P +5,-3 | 16S | 17Cl +7,-1 | 18Ar |
(2)表中不同种元素最本质的区别是______(填序号).
A.质子数不同 B.中子数不同
C.相对原子质量不同 D.电子数不同
(3)11号元素属于______元素(填“金属”或“非金属”),它在化学反应中形成的粒子与______(写元素符号)原子具有相同的核外电子排布.
(4)16号元素的原子核外电子数为______,推测该元素最低负化合价为______价,最高正化合价的氧化物的化学式为______.
(5)从化合价角度分析,我们可以发现一些规律.请写出其中的一个:______.
(6)某元素R与硫酸根形成化合物的化学式为:RSO4,其相对分子质量为152,回答下列问题:
①R的元素符号为______.
②R在化合物中可以显+3价,则+3价R的氧化物的化学式为______,+3价R的氧化物中R的质量分数是多少?(写出计算过程)