已知在溶液中氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠.现实验室中有一包白色粉末,可能是碳酸钠,也可能是氧化钙或氢氧化钙.为确定其组成,某同学设计了以下实验方案进行探究,请你按要求帮助完成探究活动.
(1)提出假设:假设①白色粉末是碳酸钠
假设②白色粉末是氧化钙
假设③白色粉末是氢氧化钙
(2)设计实验,通过实验分析进行判断并填空
(3)实验后思考:假定这包白色粉末是混有少量氧化钙的碳酸钠粉末,将混合物溶于水可观察到的现象是______;若将反应后的混合物进行固液分离,分离的方法是______;再将分离后的溶液蒸干,得到的固体物质是______(填化学式).
0 67230 67238 67244 67248 67254 67256 67260 67266 67268 67274 67280 67284 67286 67290 67296 67298 67304 67308 67310 67314 67316 67320 67322 67324 67325 67326 67328 67329 67330 67332 67334 67338 67340 67344 67346 67350 67356 67358 67364 67368 67370 67374 67380 67386 67388 67394 67398 67400 67406 67410 67416 67424 211419
(1)提出假设:假设①白色粉末是碳酸钠
假设②白色粉末是氧化钙
假设③白色粉末是氢氧化钙
(2)设计实验,通过实验分析进行判断并填空
| 假设 | 设计的相关实验操作 | 实验中观察到的现象 | 假设是否成立 |
| ① | 取一定量粉末加入稀盐酸 | 没有气体产生 | ______ |
| ② | 取一定量粉末溶于水 | 溶液浑浊且温度升高 | ______ |
③ | 取一定量粉末溶于水,静置后取上层清液再通入二氧化碳 | 没有沉淀产生 | ______ |

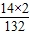 ×100%
×100%