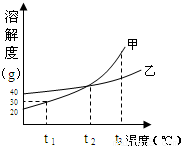
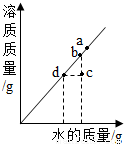
氯化钠和碳酸钠晶体的溶解度(0℃~30℃)如表所示,根据表中数据分析,下列说法错误的是( )
A.碳酸钠晶体的溶解度受温度的影响较大
B.将等质量的氯化钠和碳酸钠饱和溶液从30℃降至0℃,析出相同质量的晶体
C.氯化钠和碳酸钠晶体的溶解度相等时所对应的温度范围在20℃~30℃之间
D.除去碳酸钠浓溶液中含有的少量氯化钠,可用冷却结晶法
| 物质温度 | 0℃ | 10℃ | 20℃ | 30℃ |
| NaCl | 35.7g | 35.8g | 36.0g | 36.3g |
| Na2CO3?10H2O | 7.0g | 12.5g | 21.5g | 38.8g |
A.碳酸钠晶体的溶解度受温度的影响较大
B.将等质量的氯化钠和碳酸钠饱和溶液从30℃降至0℃,析出相同质量的晶体
C.氯化钠和碳酸钠晶体的溶解度相等时所对应的温度范围在20℃~30℃之间
D.除去碳酸钠浓溶液中含有的少量氯化钠,可用冷却结晶法
下表是硫酸溶液和氨水的密度与其溶质质量分数对照表(20℃).
请你仔细分析后回答下列问题:
(1)根据上表可总结出的规律是:对于硫酸溶液 ;
对于氨水 .
(2)某同学多次、随机抽取表中数据来探究浓、稀溶液等体积混合后,溶质质量分数与浓、稀溶液等质量混合后溶质质量分数之间的关系.
已知:将12%的硫酸溶液与28%的硫酸溶液等质量混合,所的溶液中溶质的质量分数等于a%,此a值为 .
而将12%的硫酸溶液与28%的硫酸溶液等体积混合,所得溶液中溶质的质量分数 a%(用“>”、“<”或“=”填空,下同);
将12%的氨水与28%的氨水等体积混合,所得溶液中溶质的质量分数 a%.
(3)根据以上计算或推理的结果,总结出的规律是 ;
; .
| 溶液中溶质的质量分数 | 4% | 12% | 16% | 24% | 28% |
| 硫酸溶液的密度/g?mL-1 | 1.02 | 1.08 | 1.11 | 1.17 | 1.20 |
| 氨水的密度/g?mL-1 | 0.98 | 0.95 | 0.94 | 0.91 | 0.90 |
(1)根据上表可总结出的规律是:对于硫酸溶液 ;
对于氨水 .
(2)某同学多次、随机抽取表中数据来探究浓、稀溶液等体积混合后,溶质质量分数与浓、稀溶液等质量混合后溶质质量分数之间的关系.
已知:将12%的硫酸溶液与28%的硫酸溶液等质量混合,所的溶液中溶质的质量分数等于a%,此a值为 .
而将12%的硫酸溶液与28%的硫酸溶液等体积混合,所得溶液中溶质的质量分数 a%(用“>”、“<”或“=”填空,下同);
将12%的氨水与28%的氨水等体积混合,所得溶液中溶质的质量分数 a%.
(3)根据以上计算或推理的结果,总结出的规律是 ;
; .
某工厂在装配一件设备时,不小心把一个用镁合金制造的精密空心小球掉到一个又深、又小的坚固的水泥小洞中,用各种工具都取不出来,有人提出往小洞中倒入某种溶液使小球浮起的方法.现有三种物质的溶解度数据(注:水的密度为1g/cm3,溶液的体积变化忽略不计.)
在保证不损坏小球的前提下,理论上可以用上表中 物质配制成溶液,倒入小洞中使小球浮起,该溶液的最低温度应保持在 ℃以上(已知该小球的密度为1.60g/cm3).在以上计算所得的最低温度时,该饱和溶液溶质的质量分数是 ;若小洞的容积为4000mL,要配制4000mL上述饱和溶液,理论上至少需要溶质 g.
0 65203 65211 65217 65221 65227 65229 65233 65239 65241 65247 65253 65257 65259 65263 65269 65271 65277 65281 65283 65287 65289 65293 65295 65297 65298 65299 65301 65302 65303 65305 65307 65311 65313 65317 65319 65323 65329 65331 65337 65341 65343 65347 65353 65359 65361 65367 65371 65373 65379 65383 65389 65397 211419
| 物质 | 溶解度/g | ||||
| 20℃ | 40℃ | 60℃ | 80℃ | 100℃ | |
| 硝酸铜 | 125.1 | 159.8 | 178.8 | 207.8 | 239.6 |
| 硝酸钾 | 31.6 | 64.0 | 110.0 | 169.0 | 246.0 |
| 氯化钾 | 34.0 | 40.0 | 45.0 | 51.1 | 56.7 |