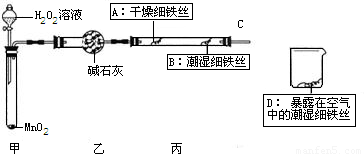
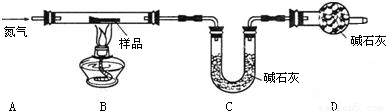
某制碱厂以岩盐水为主要原料生产纯碱(Na2CO3)和其他副产品.
(一)有关资料:
原料岩盐水主要是含NaCl,此外还含有较多Na2SO4,以及少量CaCl2和MgCl2.上述几种物质在不同温度时的溶解度数据如下表:
(1)10℃时,饱和Na2SO4溶液中溶质的质量分数是______(精确到0.1%).
(二)生产工艺

经上述处理后得到主产品:工业纯碱,副产品:A晶体.
(2)“降温”的目的是析出副产品“A晶体”,A的化学式是_______;
(3)“操作I”名称是 _______
(4)“盐水精制Ⅱ”是除去盐水中的其他杂质.反应的化学方程式是:______、______
(三)工业纯碱中杂质的判断:已知:NH4Cl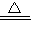 NH3↑+HCl↑
NH3↑+HCl↑
实验步骤:
①取一定质量的纯碱样品,经多次充分加热后再称重,发现质量无变化;
②另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀.
(5)由上述实验可确定纯碱样品含有杂质______(写化学式)
0 64831 64839 64845 64849 64855 64857 64861 64867 64869 64875 64881 64885 64887 64891 64897 64899 64905 64909 64911 64915 64917 64921 64923 64925 64926 64927 64929 64930 64931 64933 64935 64939 64941 64945 64947 64951 64957 64959 64965 64969 64971 64975 64981 64987 64989 64995 64999 65001 65007 65011 65017 65025 211419
(一)有关资料:
原料岩盐水主要是含NaCl,此外还含有较多Na2SO4,以及少量CaCl2和MgCl2.上述几种物质在不同温度时的溶解度数据如下表:
| 温度/℃ | 10 | 20 | 30 | 40 | ||
| 溶 解 度 /g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| Na2SO4 | 4.5 | 9.6 | 20.2 | 40.8 | 48.4 | |
| CaCl2 | 59.5 | 65.0 | 74.5 | 100 | 116 | |
| MgCl2 | 52.9 | 53.8 | 54.8 | 56.0 | 58.0 | |
(二)生产工艺

经上述处理后得到主产品:工业纯碱,副产品:A晶体.
(2)“降温”的目的是析出副产品“A晶体”,A的化学式是_______;
(3)“操作I”名称是 _______
(4)“盐水精制Ⅱ”是除去盐水中的其他杂质.反应的化学方程式是:______、______
(三)工业纯碱中杂质的判断:已知:NH4Cl
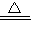 NH3↑+HCl↑
NH3↑+HCl↑实验步骤:
①取一定质量的纯碱样品,经多次充分加热后再称重,发现质量无变化;
②另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀.
(5)由上述实验可确定纯碱样品含有杂质______(写化学式)