水和溶液在生命活动和生产、生活中起着十分重要的作用.
(1)净水器中常用到活性炭,其作用是 .
(2)水常用来配制各种溶液,氯化铁溶液中的溶质为 (写化学式).
(3)农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种.现将300g 25%的NaCl溶液稀释为15%的NaCl溶液,稀释后溶液的质量为 g.
(4)根据下表回答问题.
①40℃时,向两个分别盛有40g NaCl和NH4Cl的烧杯中,各加入100g的水,充分溶解后,为不饱和溶液的是 溶液.
②采用一种操作方法,将上述的不饱和溶液变为饱和溶液.下列说法正确的是 (填字母序号).
A.溶质的质量一定不变 B.溶液中溶质的质量分数一定增大
C.溶液质量可能不变 D.可升高温度或减少溶剂.
(1)净水器中常用到活性炭,其作用是 .
(2)水常用来配制各种溶液,氯化铁溶液中的溶质为 (写化学式).
(3)农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种.现将300g 25%的NaCl溶液稀释为15%的NaCl溶液,稀释后溶液的质量为 g.
(4)根据下表回答问题.
| 温度/℃ | 20 | 40 | 60 | 80 | 100 | ||
| 溶解度 /g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |
②采用一种操作方法,将上述的不饱和溶液变为饱和溶液.下列说法正确的是 (填字母序号).
A.溶质的质量一定不变 B.溶液中溶质的质量分数一定增大
C.溶液质量可能不变 D.可升高温度或减少溶剂.
铜、铁、锌是三种常见的金属,请回答下列问题.
(1)细铁丝在氧气中能发生燃烧,反应的化学方程式为 .
(2)铁粉和水蒸气在加热时生成四氧化三铁和氢气,该反应的基本反应类型为 .
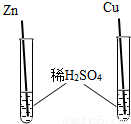
(3)小强同学为了验证Zn、Cu的金属活动性强弱,设计了如下方案,其中能达到实验目的是 (填序号).
(4)向铜粉和铁粉的混合物中加入一定量的盐酸,充分反应后过滤.以下判断正确的是 (填序号).
A.滤纸上一定没有铜
B.滤纸上可能含有铁
C.滤液中可能含有盐酸
D.滤液中一定含有氯化亚铁
(5)铜在一定条件下也会生锈.某化学兴趣小组用A~D装置探究铜生锈的条件(A、B、D中均为煮沸过的蒸馏水,B中试管上层充满CO2,C中放有干燥剂,D中通一段时间空气后将试管密封).
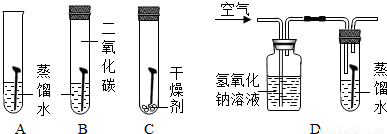
十天后发现,只有A中铜生锈,且水面处铜生锈较严重.
①B中发生反应的化学方程式为 .
②铜生锈的条件是 .
(1)细铁丝在氧气中能发生燃烧,反应的化学方程式为 .
(2)铁粉和水蒸气在加热时生成四氧化三铁和氢气,该反应的基本反应类型为 .
(3)小强同学为了验证Zn、Cu的金属活动性强弱,设计了如下方案,其中能达到实验目的是 (填序号).
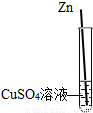 | 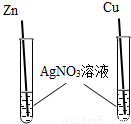 | 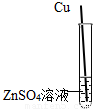 |  |
| A | B | C | D |
A.滤纸上一定没有铜
B.滤纸上可能含有铁
C.滤液中可能含有盐酸
D.滤液中一定含有氯化亚铁
(5)铜在一定条件下也会生锈.某化学兴趣小组用A~D装置探究铜生锈的条件(A、B、D中均为煮沸过的蒸馏水,B中试管上层充满CO2,C中放有干燥剂,D中通一段时间空气后将试管密封).

十天后发现,只有A中铜生锈,且水面处铜生锈较严重.
①B中发生反应的化学方程式为 .
②铜生锈的条件是 .
某化学兴趣小组对水蒸气通过灼热的焦炭后,得到的混合气体主要成分产生了兴趣.同学们决定通过实验进行探究.
[提出猜想]该混合气体主要成分为一氧化碳、二氧化碳、氢气和水蒸气.
[查阅资料]a.无水硫酸铜遇水由白色变为蓝色.
b.碱石灰是固体氢氧化钠和氧化钙的混合物.
c.氢气、一氧化碳均能在加热的条件下与氧化铜反应.
[实验过程]同学们在老师的指导下设计了如图所示装置,并进行了实验(部分夹持仪器已略去).
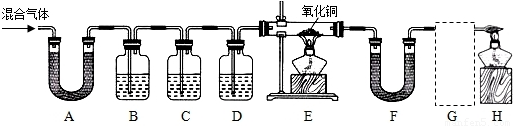
(1)装置A中无水硫酸铜变蓝,装置B中澄清石灰水变浑浊.由此得出的结论为______.写出装置B中反应的化学方程式______.
(2)装置C和D中的药品分别为______.
(3)同学们通过观察装置E、F中的现象后,证明了混合气中含有氢气.为了证明第四种气体的存在,装置G中的药品、现象和结论是______.
[实验结论]猜想正确.
[实验反思]
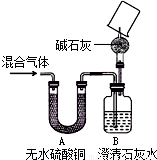
经过讨论,同学们将上图中装置C~H进行了简化,改进后的装置如图所示.
(3)干燥管中碱石灰的作用为______.
(4)同学们为了验证通过干燥管后气体的成分,继续进行的实验为:
[提出猜想]该混合气体主要成分为一氧化碳、二氧化碳、氢气和水蒸气.
[查阅资料]a.无水硫酸铜遇水由白色变为蓝色.
b.碱石灰是固体氢氧化钠和氧化钙的混合物.
c.氢气、一氧化碳均能在加热的条件下与氧化铜反应.
[实验过程]同学们在老师的指导下设计了如图所示装置,并进行了实验(部分夹持仪器已略去).

(1)装置A中无水硫酸铜变蓝,装置B中澄清石灰水变浑浊.由此得出的结论为______.写出装置B中反应的化学方程式______.
(2)装置C和D中的药品分别为______.
(3)同学们通过观察装置E、F中的现象后,证明了混合气中含有氢气.为了证明第四种气体的存在,装置G中的药品、现象和结论是______.
[实验结论]猜想正确.
[实验反思]
经过讨论,同学们将上图中装置C~H进行了简化,改进后的装置如图所示.
(3)干燥管中碱石灰的作用为______.
(4)同学们为了验证通过干燥管后气体的成分,继续进行的实验为:
| 实验操作 | 实验现象 | 实验结论 | |
| ① | 在尖嘴处点燃气体, ______. | ______. | ______. |
| ② | ______. | ______. | ______. |

为测定某大理石样品中碳酸钙(杂质不溶于水也不参与反应)的质量分数,某小组的同学进行了如下实验(水和氯化氢的挥发忽略不计):取12.5g样品研碎放入烧杯中,每次加入20.8g稀盐酸后并用电子天平称量,记录实验数据如下.
请计算:
(1)大理石样品中碳酸钙的质量分数.
(2)恰好完全反应时烧杯内溶液的溶质质量分数.
0 64034 64042 64048 64052 64058 64060 64064 64070 64072 64078 64084 64088 64090 64094 64100 64102 64108 64112 64114 64118 64120 64124 64126 64128 64129 64130 64132 64133 64134 64136 64138 64142 64144 64148 64150 64154 64160 64162 64168 64172 64174 64178 64184 64190 64192 64198 64202 64204 64210 64214 64220 64228 211419
| 加入稀盐酸次数 | 1 | 2 | 3 | 4 | 5 |
| 烧杯及所称物质总质量/g | 72.2 | 91.9 | 111.6 | 131.3 | 152.1 |
(1)大理石样品中碳酸钙的质量分数.
(2)恰好完全反应时烧杯内溶液的溶质质量分数.

 H2O+CO2↑+CO↑.
H2O+CO2↑+CO↑.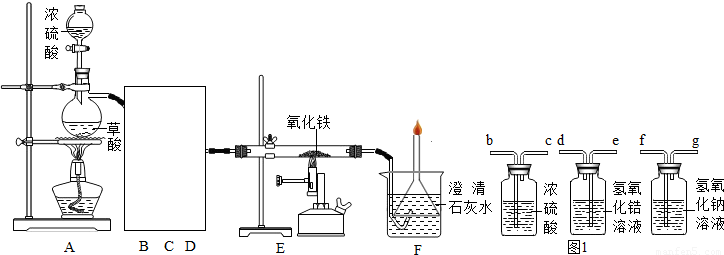
 C2H4+4H2O.若用24g H2转化CO2,则理论上能生成C2H4的质量为多少克?
C2H4+4H2O.若用24g H2转化CO2,则理论上能生成C2H4的质量为多少克?