现有生活中常见的四种未知白色粉末,它们分别是食盐、纯碱、去污粉(主要成分为碳酸钠和碳酸钙)和使用过的生石灰干燥剂.化学小组为了确定每种未知固体的成分,将它们分别标记为①、②、③、④后进行实验,实验现象记录如下:
根据以上实验现象,回答下列问题:
(1)实验1中,物质①发生反应的化学方程式是______.
(2)物质②为______,试剂A为______.
(3)物质③为______.
(4)通过实验判断,物质①中一定含有的成分是______.
| 实验过程 | 实验现象 |
| 实验1:分别取样于四支试管中,加入足量的水充分溶解 | ②、③完全溶解,①、④均在试管底部有白色固体,且①中有明显放热 |
| 实验2:静置一段时间后,分别取上层清液,加入试剂A | ③、④均有气泡产生 |
| 实验3:分别取样于四支试管中,加入足量试剂A | 白色固体均消失;①③④均有气泡产生 |
(1)实验1中,物质①发生反应的化学方程式是______.
(2)物质②为______,试剂A为______.
(3)物质③为______.
(4)通过实验判断,物质①中一定含有的成分是______.
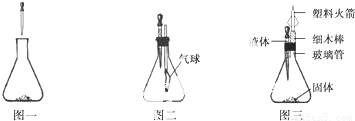
生活中用到各种漂白剂.化学课上,老师带来一种常用作氧系漂白剂的物质,可能是双氧水(H2O2)、过碳酸钠和过氧化钙(CaO2)中的一种.同学们观察发现,该漂白剂为白色粉末(右图).
【提出猜想】该漂白剂肯定不是 .
【查阅资料】①过碳酸钠是一种白色结晶颗粒,溶于水时,迅速分解生成碳酸钠和过氧化氢.
②过氧化氢常温下不稳定,实验室用过氧化氢制取氧气的化学方程式为 .
③过氧化钙,白色固体,难溶于水.与水反应缓慢释放氧气,同时生成一种碱,反应的化学方程式为 .
【实验验证】同学们设计了下列实验方案进行验证,请将方案的空格填写完整.
【交流反思】小组讨论时,小欢认为根据步骤1、3即可确定白色固体的成分,不需要进行步骤2,你认为她的意见 (填“合理”或“不合理”),理由是 .

【提出猜想】该漂白剂肯定不是 .
【查阅资料】①过碳酸钠是一种白色结晶颗粒,溶于水时,迅速分解生成碳酸钠和过氧化氢.
②过氧化氢常温下不稳定,实验室用过氧化氢制取氧气的化学方程式为 .
③过氧化钙,白色固体,难溶于水.与水反应缓慢释放氧气,同时生成一种碱,反应的化学方程式为 .
【实验验证】同学们设计了下列实验方案进行验证,请将方案的空格填写完整.
| 实验步骤 | 实验操作 | 实验现象 | 结论 |
| 步骤1 | 取2g白色固体放入试管中,加入20mL水,充分振荡. | 液体浑浊, 有持续的细小气泡冒出. | |
| 步骤2 | 静置,取步骤1的试管上层清液少许,滴加无色酚酞. | 无色酚酞变红. | |
| 步骤3 | 该消毒剂的成分不是过碳酸钠. |

化学实验小组的同学要测定从商店买来的某品牌纯碱中碳酸钠的质量分数(已知杂质为NaCl),经过讨论,他们设计并进行了如下实验(反应过程中不考虑水和氯化氢的挥发):
取13.5g样品放入烧杯中,每次加入20g稀盐酸(不考虑水、氯化氢逸出)后用精密仪器称量,记录实验数据如下:
(1)第______次加入稀盐酸后样品完全反应.
(2)请你帮助他们计算出样品中碳酸钠的质量分数.
(3)求样品与稀盐酸恰好完全反应时所得溶液中溶质的质量分数.
0 63256 63264 63270 63274 63280 63282 63286 63292 63294 63300 63306 63310 63312 63316 63322 63324 63330 63334 63336 63340 63342 63346 63348 63350 63351 63352 63354 63355 63356 63358 63360 63364 63366 63370 63372 63376 63382 63384 63390 63394 63396 63400 63406 63412 63414 63420 63424 63426 63432 63436 63442 63450 211419
取13.5g样品放入烧杯中,每次加入20g稀盐酸(不考虑水、氯化氢逸出)后用精密仪器称量,记录实验数据如下:
| 加入稀盐酸次数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 烧杯及所称物质总质量/g | 78.90 | 97.80 | 116.70 | 135.60 | 155.05 | 175.05 | 195.05 |
(2)请你帮助他们计算出样品中碳酸钠的质量分数.
(3)求样品与稀盐酸恰好完全反应时所得溶液中溶质的质量分数.