某学生分别用1g的铁屑、锌粒、镁片与足量的某酸反应以制取氢气,完全反应所需时间与当地的金属价格如下表所示.
你认为实验室中一般不选用铁屑、镁片与酸反应制取氢气的主要原因是什么?
| 物 质 | 所需时间 | 价 格 |
| 铁屑 | 约13900s | 10.00元/1000g |
| 锌粒 | 约50s | 20.00元/500g |
| 镁片 | 约20s | 10.80元/25g |
某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如图所示的装置进行探究.
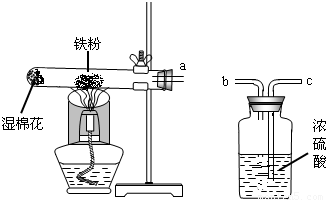
(1)已知试管内湿棉花不参加化学反应,它的作用是______;
(2)若干燥从a导管出来的气体,应从______(选填“b”或“c”)端管口通入;
(3)对化学变化过程中生成的气体同学们有以下猜想:
猜想一:生成的气体可能是氢气;猜想二:生成的气体可是______.
(4)请你对猜想二进行探究:
(5)其实红热的铁遇到水蒸气,在生成气体的同时,还会生成一种黑色固体.你认为生成的黑色固体可能是______.

(1)已知试管内湿棉花不参加化学反应,它的作用是______;
(2)若干燥从a导管出来的气体,应从______(选填“b”或“c”)端管口通入;
(3)对化学变化过程中生成的气体同学们有以下猜想:
猜想一:生成的气体可能是氢气;猜想二:生成的气体可是______.
(4)请你对猜想二进行探究:
| 操作方法 | 现象 | 结论 |
| ______ | ______ | ______ |
某化学兴趣小组用化学方法测定一种钢样品中铁的含量.同学们称取了5.7g钢样品,投入装有10.0g稀盐酸(足量)的烧杯(烧杯质量也为10.0g)中.在化学反应过程中对烧杯(包括溶液和残余固体)进行了四次称量,记录如下表:
(1)反应中产生氢气______克,这种钢样品中铁的含量是多少?(精确到0.1%)______
(2)钢的类型分为:含碳质量(C%)0.03%~0.3%为低碳钢;0.3%~0.6%为中碳钢;0.6%~2%为高碳钢.假设残留在烧杯中的黑色固体全部是炭,则这种钢属于______.
(3)有同学提出:灼烧可使钢中的炭变为CO2挥发掉,灼烧后钢样品质量会减轻.可是他们将一定量的钢样品灼烧后,发现质量反而增加了很多.原因是______.
0 63238 63246 63252 63256 63262 63264 63268 63274 63276 63282 63288 63292 63294 63298 63304 63306 63312 63316 63318 63322 63324 63328 63330 63332 63333 63334 63336 63337 63338 63340 63342 63346 63348 63352 63354 63358 63364 63366 63372 63376 63378 63382 63388 63394 63396 63402 63406 63408 63414 63418 63424 63432 211419
| 反应时间 | t | t1 | t2 | t3 |
| 烧杯和药品质量/g | 25.7 | 25.6 | 25.5 | 25.5 |
(2)钢的类型分为:含碳质量(C%)0.03%~0.3%为低碳钢;0.3%~0.6%为中碳钢;0.6%~2%为高碳钢.假设残留在烧杯中的黑色固体全部是炭,则这种钢属于______.
(3)有同学提出:灼烧可使钢中的炭变为CO2挥发掉,灼烧后钢样品质量会减轻.可是他们将一定量的钢样品灼烧后,发现质量反而增加了很多.原因是______.