将固体FeC2O4?2H2O放在可称出质量的容器内加热,FeC2O4?2H2O首先逐步失去结晶水,温度继续升高时,FeC2O4会逐渐转变为铁的氧化物:Fe3O4、Fe2O3、FeO.现称取2.00g FeC2O4?2H2O,持续加热,剩余固体的质量随温度变化的部分数据见下表:
根据上述数据计算推断:
(1)300℃~350℃时,固体物质质量不变的原因是 ;
(2)400℃~450℃内的固体物质的化学式为 ;
(3)500℃~600℃内的固体物质的化学式为 ;
(4)700℃~800℃内的固体物质的化学式为 .
| 温度/℃ | 25 | 150 | 300 | 350 | 400 | 450 | 500 | 600 | 700 | 800 |
| 固体质量/g | 2.000 | 1.804 | 1.600 | 1.600 | 0.800 | 0.800 | 0.888 | 0.888 | 0.860 | 0.860 |
(1)300℃~350℃时,固体物质质量不变的原因是 ;
(2)400℃~450℃内的固体物质的化学式为 ;
(3)500℃~600℃内的固体物质的化学式为 ;
(4)700℃~800℃内的固体物质的化学式为 .
在酸性条件下,次氯酸钠(NaClO)、过氧化氢(H2O2)都有很强的氧化性,可将Fe2+氧化为Fe3+;在溶液中,Mg(OH)2和Fe(OH)2呈胶状物或絮状物沉淀;而MgCO3在水中煮沸可转化为更难溶的Mg(OH)2.
“卤块”的主要成分为MgCl2,还含有FeCl2、FeCl3、MnCl2等杂质.若以它为原料,按图所示的工艺流程即可制得“轻质氧化镁”.并要求产品尽量不含杂质离子,而且成本较低,流程中加入的物质及其pH控制,都可参考下表1、表2来确定.

表1 生成氢氧化物沉淀时的pH
表2工业品价格
请根据以上信息填写下列空白:
(1)写出在盐酸溶液中,NaClO将FeCl2氧化成FeCl3,同时生成NaCl和水的化学方程式______;
同时H2O2将FeCl2氧化成FeCl3,并生成了水,其化学方程式______.
(2)在步骤②中加入的物质X,最佳的选择应是______,理由是______.
(3)在步骤③中加入的物质Y应是______,之所以要控制pH=9.8,其目的是______.
(4)在步骤④中加入的物质Z应是______.
(5)在步骤⑤时发生的化学反应方程式是______ Mg(OH)2+CO2↑
“卤块”的主要成分为MgCl2,还含有FeCl2、FeCl3、MnCl2等杂质.若以它为原料,按图所示的工艺流程即可制得“轻质氧化镁”.并要求产品尽量不含杂质离子,而且成本较低,流程中加入的物质及其pH控制,都可参考下表1、表2来确定.

表1 生成氢氧化物沉淀时的pH
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
| 工业品 | 规格 | 价格(元.╱吨) |
| 漂液 | 含NaClO 25.2% | 450 |
| 过氧化氢 | 含H2O230% | 240 |
| 烧碱 | 含NaOH 98.5% | 2100 |
| 纯碱 | 含Na2CO399.5% | 600 |
| 卤块 | 含MgCl2 30% | 310 |
(1)写出在盐酸溶液中,NaClO将FeCl2氧化成FeCl3,同时生成NaCl和水的化学方程式______;
同时H2O2将FeCl2氧化成FeCl3,并生成了水,其化学方程式______.
(2)在步骤②中加入的物质X,最佳的选择应是______,理由是______.
(3)在步骤③中加入的物质Y应是______,之所以要控制pH=9.8,其目的是______.
(4)在步骤④中加入的物质Z应是______.
(5)在步骤⑤时发生的化学反应方程式是______ Mg(OH)2+CO2↑
根据下列所给出的药品、实验装置和实验中可测得的数据,设计实验来粗略测定由铜和锌两种金属组成的合金a g中锌的质量分数(合金已加工成粉末).
药品:足量的浓硫酸、足量的稀硫酸、足量的稀硝酸和氧化铜.
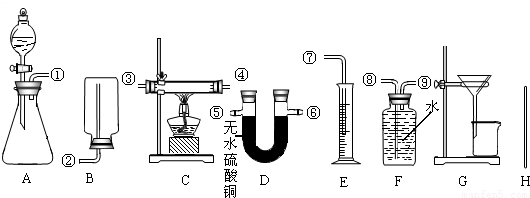
在实验中可测得的数据:
充分反应后,生成氢气的体积为bL(在此条件下,2.0gH2的体积是22.4L),反应前仪器和药品的质量为c g,充分反应后剩余固体的质量为d g,充分反应后仪器和药品的质量为e g.请你设计三个方案填入下表中:
0 62713 62721 62727 62731 62737 62739 62743 62749 62751 62757 62763 62767 62769 62773 62779 62781 62787 62791 62793 62797 62799 62803 62805 62807 62808 62809 62811 62812 62813 62815 62817 62821 62823 62827 62829 62833 62839 62841 62847 62851 62853 62857 62863 62869 62871 62877 62881 62883 62889 62893 62899 62907 211419
药品:足量的浓硫酸、足量的稀硫酸、足量的稀硝酸和氧化铜.

在实验中可测得的数据:
充分反应后,生成氢气的体积为bL(在此条件下,2.0gH2的体积是22.4L),反应前仪器和药品的质量为c g,充分反应后剩余固体的质量为d g,充分反应后仪器和药品的质量为e g.请你设计三个方案填入下表中:
| 选用药品的名称(1) | 选用的实验装置及组装时接口的连接顺序(2) | 需测得的实验数据(从上述可测得的数据中选取)(3) | 合金中锌的质量分数的计算式(4) | ||
| 选用的实验装置序号 | 组装时接口编号的连接顺序(如不需要组装,则不填) | ||||
| 方案一 | |||||
| 方案二 | |||||
| 方案三 | |||||
 某市环保部门绘制的四年来该地区全年降雨的平均pH变化示意图,请回答下列问题:
某市环保部门绘制的四年来该地区全年降雨的平均pH变化示意图,请回答下列问题: