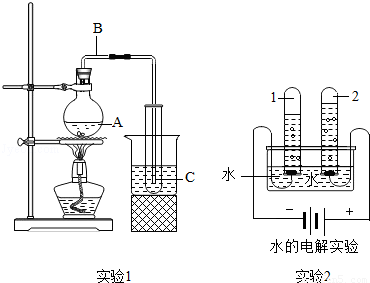
某兴趣小组做了如下实验.
【实验一】提纯NaCl
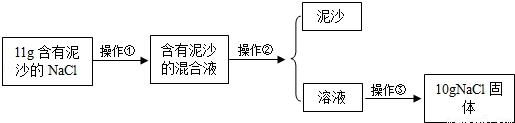
请根据实验回答下列问题:
(1)操作①、②、③依次为下图中的(填序号) .
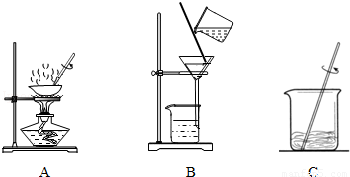
(2)若得到NaCl的产率比实际值偏低,则可能的原因是(填序号) .
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.把晶体从蒸发皿转移到天平上称量时,有少量粘在了蒸发皿上
D.溶解11g含有泥沙的NaCl时,加入的水量不足
(3)用上述实验所得的氯化钠配制溶质质量分数为5%的氯化钠溶液50g,不需要的仪器为(填序号) .
A.量筒 B.天平 C.烧杯 D.漏斗 E.蒸发皿 F.玻璃棒 G.酒精灯
【实验二】溶解和结晶KNO3
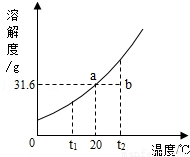
请根据实验和KNO3溶解度曲线回答下列问题(水的密度以1g/mL计):
|
实验操作 |
实验结果 |
|
取100mL水,加入25gKNO3,搅拌,20℃ |
全部溶解,得溶液① |
|
再加Xg KNO3,搅拌,20℃ |
恰好饱和,得溶液② |
|
再加25g KNO3,搅拌,20℃ |
得溶液③ |
|
加热 |
全部溶解,得溶液④ |
|
冷却至20℃ |
晶体析出,得溶液⑤ |
(4)溶液③的质量为 ;一定属于不饱和溶液的是(填数字序号) ;溶质的质量分数一定相等的是(填序号) .
(5)析出晶体的质量为(填序号) .
A.25g B.X+25g C.X+100g.
实验室里,试剂瓶的标签常因脱落或被腐蚀而丢失,现有失去标签的6瓶溶液,可能是NaCl、Na2CO3、NaOH、CaCl2、Ca(OH)2、HCl、CuSO4七种物质中的六种,教师将它们编号为A、B、C、D、E、F,让同学们鉴别这六种物质,请你参与小明的下列鉴别过程.
[查阅资料]:CaCl2溶液显中性,CaCl2+Na2CO3=CaCO3↓+2NaCl
(1)观察各种溶液的颜色,其中C瓶为 色,是硫酸铜溶液.
(2)做两两混合实验,E与其他四种物质混合的实验现象记录如下:
|
|
A |
B |
D |
F |
|
E |
无现象 |
白色沉淀 |
无色气泡 |
白色沉淀 |
由此实验确定 E是 (写化学式),还能确定 .
(3)若只用酚酞溶液,进一步确定另外三种物质的成分,你的实验设计是(填下表):
|
实验操作 |
实验现象及实验结论 |
|
|
|
(4)六种物质都鉴别出来以后,小明将NaOH溶液和Na2CO3溶液混合,再滴加稀盐酸,从开始滴加稀盐酸到过量的现象是 ;此时溶液中的溶质为 .
CaO和NaOH固体的混合物,俗名“碱石灰”,实验室常用作干燥剂.碱石灰在空气久置会吸收空气中的水和二氧化碳而变质.某实验小组为确定一瓶久置的碱石灰样品的成分,设计了如图所示实验流程. 请你参与探究过程:
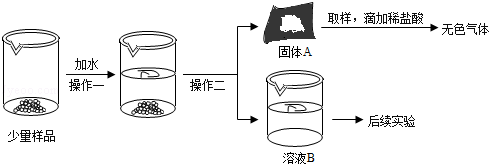
(1)为了使样品充分溶解,操作一定还要用到的玻璃仪器是 ;操作二的名称是 .
(2)固体A中一定含有 .
(3)溶液B成分的探究.
[查阅资料]
①Ca(OH)2、Na2CO3溶于水无明显的温度变化;
②Na2CO3溶液呈碱性,能使酚酞试液变红;
③CaCl2溶液呈中性.
[猜想]
溶液B中溶质可能为:①NaOH; ②Na2CO3; ③NaOH和Na2CO3;④Ca(OH)2和
[设计方案并进行实验]
甲、乙同学分别设计如下方案并进行探究:
甲同学:取少量溶液B于试管中,滴加足量的稀盐酸,产生大量气泡,则溶液B中的溶质是Na2CO3.
乙同学:取少量溶液B于试管中,滴加几滴酚酞试液,溶液变成红色,则溶液B中的溶质一定含有NaOH.
[反思与评价]
丙同学认真分析上述二位同学的实验,认为他们的结论均有不足之处,并且做出了正确的判断.他认为B溶液中一定含有Na2CO3,可能含有NaOH.为进一步确认溶液B中是否含NaOH,做做了如下实验.
|
实验步骤 |
实验现象 |
实验结论 |
|
①取少量溶液B于试管中,加入足量CaCl2溶液; ②过滤,在滤液中滴加酚酞试液 |
①有白色沉淀生成 ②溶液由无色变为红色 |
猜想③正确 |
实验步骤①中发生的化学反应方程式是 ,其实验目的是 .
(4)实验过程中,同学们发现向样品中加水时还放出大量的热.综合以上探究,下列对样品成分分析正确的是 (填序号).
A.一定有NaOH B.一定有Na2CO3 C.一定有CaO D.至少有NaOH、CaO中的一种.

 Cu+H2O)
Cu+H2O)