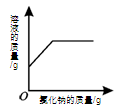
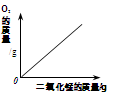某同学在四个烧杯中分别做氯化铵(NH4Cl)溶解实验。依据表格中的数据回答
问题。
|
烧杯序号 |
温度/℃ |
水的质量/g |
氯化铵质量/g |
溶液质量/g |
|
① |
20 |
100 |
20 |
a |
|
② |
20 |
100 |
40 |
137.2 |
|
③ |
40 |
100 |
40 |
140 |
|
④ |
60 |
100 |
50 |
150 |
(1)a为 。
(2)20℃时,氯化铵的溶解度是 g,
(3)将烧杯①所得溶液稀释成溶质的质量分数为10%的溶液,需要加水 g。
(4)上述烧杯中的溶液不能确定是否达到饱和状态的是 (填烧杯序号)。
(5)若使烧杯②溶液中溶质的质量分数增大,可继续 (填字母序号)。
A加水;B加入少量氯化铵;C恒温蒸发部分溶剂;D升温到40℃;E.加入100g60℃时氯化铵的饱和溶液,再恢复至20℃
A、B为初中化学常见物质,它们分别由H、C、O、Cl、Ca、Mn中的一种或几种元素组成。用下图装置(图中铁架台等仪器均已略去)进行实验。实验步骤如下:
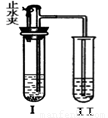
(1)若在I中加入一定量固体A和液体B后,塞紧橡皮塞,立即打开止水夹,发现Ⅱ中有气泡冒出。则A、B可能为(至少写出符合要求的2组物质)
|
A |
|
|
|
|
B |
|
|
|
友情提示:填写物质的化学式、名称或俗称。
(2)若一段时间后,关闭止水夹,发现Ⅱ中液面上升,且溶液由浑浊变澄清。则Ⅱ中原液体是 ,整个实验过程中,Ⅱ中发生反应的化学方程式为 。
某化学小组测定空气中氧气的体积分数。
(1)根据右图回答问题。

①红磷燃烧的化学方程式为 。
②若将红磷改为木炭,反应结束后降至室温,打开止水夹,烧杯中的水不倒吸入集气瓶的原因是 _。
(2)用四硫化钠(Na2S4)固体可替代红磷测定空气中氧气的体积分数。
反应原理为:2Na2S4+O2+2H2O=8S↓+4NaOH(氢氧化钠)。
小资料:四硫化钠(Na2S4)与氧气、水反应生成难溶于水的固体硫(S)和易溶于水
的氢氧化钠。
【实验过程】
①取足量的四硫化钠固体加入试管中,再加入适量的水,迅速塞紧橡胶塞,充分振荡。测量液面至橡胶塞下沿的距离,记录数据h1(如图1所示)。

图1 图2
②将该试管插入水中(如图2所示),拔下橡胶塞,观察到 ,塞紧橡胶塞。将试管取出,倒转过来,测量液面至橡胶塞下沿的距离,记录数据h2。理论上h2∶h1= 。
③按照①和②再重复实验2次。3次实验数据如下表所示。
|
|
第1次 |
第2次 |
第3次 |
|
h1/cm |
11.0 |
11.4 |
11.6 |
|
h2/cm |
8.7 |
9.1 |
9.2 |
根据第3次实验数据,计算空气中氧气的体积分数为 %(结果精确到 0.1%)。
某兴趣小组同学阅读课外资料得知:很多因素都能影响过氧化氢分解速度。于是,
同学们探究影响过氧化氢分解速度的某种因素。
【实验过程】实验数据记录如下:
|
|
过氧化氢溶液的质量 |
过氧化氢溶液的浓度 |
MnO2的质量 |
测量数据 |
|
Ⅰ |
50.0g |
1% |
0.1g |
9 mL |
|
Ⅱ |
50.0g |
2% |
0.1g |
16 mL |
|
Ⅲ |
50.0g |
4% |
0.1g |
31 mL |
【实验分析】
(1)过氧化氢分解的化学方程式为 。
(2)表格中的“测量数据”的指的是:相同时间内 _。
(3)本实验中,测量O2体积的装置是 (填编号)。

【实验结论】
在相同条件下 。
【交流评价】
(1)甲同学提出在上述实验中测量 同样能得出相同的结论。
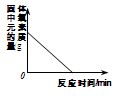
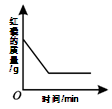
(2)乙同学提出用下图装置进行实验,通过比较 也能达到实验目的。

【实验反思】
除了上述因素会影响过氧化氢分解速度外, _(写一种)也会影响过氧化氢分解速度,你的实验方案是 。