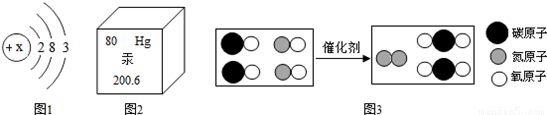
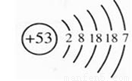
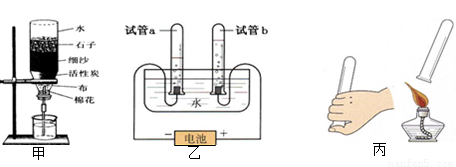
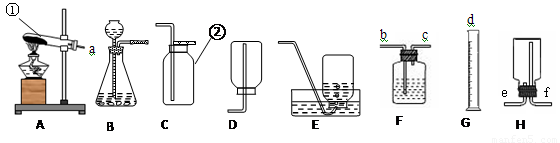“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
【实验探究一】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,催化效果如何?
实验步骤 实验现象
I.分别量取5mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 A试管中产生气泡,带火星木条复燃,B试管中无明显现象
II.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 试管中均产生气泡,带火星木条均复燃
III.将实验II中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag。
IV分别量取5mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。
【实验结论】
(1)由实验Ⅰ你可以得出的结论是 ;
(2)实验II、III证明:氧化铁的 和 在反应前后均没有发生变化,可以作过氧化氢分解的催化剂;
(3)写出氧化铁催化过氧化氢分解的符号表达式 ;
【实验评价】
(4)若实验IV观察到D试管中产生气泡的速率更快,由此你可以得到的结论是 。
【实验探究二】影响化学反应的速率除了催化剂以外,还有其它因素吗?以下是另一实验小组探究影响反应速率部分因素的相关实验数据。
|
实验序号 |
H2O2溶 液浓度% |
H2O2溶液体积/mL |
温度℃ |
MnO2的用量/g |
收集氧气的体积/mL |
反应所需 的时间/s |
|
① |
5 |
1 |
20 |
0.1 |
4 |
16.75 |
|
② |
15 |
1 |
20 |
0.1 |
4 |
6.04 |
|
③ |
30 |
5 |
35 |
0 |
2 |
49.21 |
|
④ |
30 |
5 |
55 |
0 |
2 |
10.76 |
(5)通过实验①和②对比可知,化学反应速率还与 有关;从实验 和 对比可知,化学反应速率与温度的关系是: ;
(6)化学反应的实质是微观粒子相互接触、碰撞的结果,化学反应速率与微观粒子的概率有关。试从微观角度解释“反应物浓度越大,化学反应速率越快”的原因是: 。
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2)。该维C泡腾片是 (填纯净物或混合物)

该小组同学对该气体的成分进行如下探究。
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、N2。
小明说:不可能含有N2,因为
_________________________________________。
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,而CO有剧毒。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
【进行实验】
|
实验编号 |
实验操作 |
实验现象 |
|
① |
将气体通入澄清的石灰水中 |
澄清石灰水变浑浊 |
|
② |
将带火星的木条伸入该气体中 |
带火星的木条没有复燃 |
【得出结论】(1)由实验①可知,该气体中肯定含有 。
(2)由实验②_____________(填“能”或“不能”)确定该气体中不含氧气,理由是_____________________________________________________________________________。