室温下,称取氯化钠固体和碳酸钠固体各30 g放入同一烧杯中,加入100 g水充分搅拌后静置,得到二者的混合溶液。请参照氯化钠、碳酸钠两物质的溶解度表判断,以下结论不正确的是(?? )
?????????????? 温度/℃ ?????? 溶解度/g 物质 | 0 | 10 | 20 | 30 | 40 |
氯化钠 | 35 | 35.5 | 36 | 36.5 | 37 |
碳酸钠 | 6 | 10 | 18 | 36.5 | 50 |
A.20 ℃时,氯化钠的溶解度大于碳酸钠的溶解度
B.20 ℃时,未溶解固体是氯化钠和碳酸钠的混合物
C.30 ℃时,溶液中氯化钠和碳酸钠的质量分数相同
D.30 ℃时,溶液为氯化钠和碳酸钠的不饱和溶液
下表是KNO3在不同温度时的溶解度,请回答下列问题。

温度℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
(1)分析表中数据,归纳出KNO3的溶解度随温度变化的规律___________。
(2)20 ℃时,在装有5 g KNO3晶体的试管中,加入10 g水并充分振荡,此时所得溶液为____________(选填“饱和”或“不饱和”)溶液。再将该试管放入盛有热水的烧杯中,使试管内溶液温度升至60 ℃,此时试管内的溶液中溶质与溶剂的质量比为________________。
(3)配制一定溶质质量分数的KNO3溶液时,溶解过程所需要的仪器有_________、___________________。
溶解度可表示物质溶解性的大小。
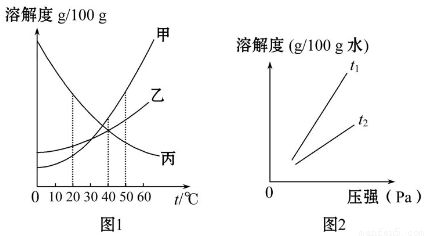
(1)如图1是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。
Ⅰ.40 ℃时,乙和丙___________(填“能”或“不能”)形成溶质质量分数相同的饱和溶液。
Ⅱ.20 ℃时,烧杯中分别盛有相同质量甲、乙、丙的饱和溶液,各加入等质量的对应固体,并升温至50 ℃。请填表:
烧杯中的溶质 | 烧杯中固体的变化 |
甲 |
|
乙 | 固体逐渐减少至全部溶解 |
丙 |
|
(2)Ⅰ.打开可乐瓶,逸出大量气体,由此可见,压强越小,CO2的溶解度越______,若要加大二氧化碳溶解的量可采用的一种方法是____________________。
Ⅱ.不同温度下,氧气的溶解度随压强的变化如图2所示,图中t1对应的温度为40 ℃,则t2对应的温度___________(填序号)。
a.大于40 ℃????????? b.小于40 ℃???????? c.无法确定
在两支试管中各加入2 mL水,然后分别加入1~2小粒碘或高锰酸钾,振荡,观察现象;然后再向两支试管中分别加1 mL汽油,振荡,静置,观察现象。记录如表所示:
溶? 剂 | 溶? 质 | 现? 象 |
先加水 | 碘 | 底部仍有碘固体,液体呈浅黄色 |
先加水 | 高锰酸钾 | 底部无固体,溶液呈深紫色 |
再加汽油 | 碘 | 分层,上层呈深紫色,下层近无色,底部无固体 |
再加汽油 | 高锰酸钾 | 分层,上层无色,下层呈深紫色,底部无固体 |
请回答:
(1)加入汽油后,投入碘的试管的上层液体名称是_________;投入高锰酸钾的试管的下层液体的名称是_____________________。
(2)从实验现象可以归纳:碘的溶解性为______________,高锰酸钾的溶解性为____________________。
(3)在科学研究中,若将大量水中溶解的少量碘“富集”起来,你认为可以采取的方法是__________________。



