期末化学实验老师整理药品时,拿出一瓶久置的氢氧化钙粉末[Ca(OH)2],他让小刘和小赵对这瓶氢氧化钙粉末的组成进行实验探究。
(1)提出问题:这瓶氢氧化钙是否已经生成碳酸钙(CaCO3)而变质?
(2)进行猜想:A:氢氧化钙全部变为碳酸钙;B:氢氧化钙部分变为碳酸钙;C:氢氧化钙没有变质。(3)设计实验方案、进行实验:下表是对猜想A进行实验探究的过程示例:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样,加适量水,搅拌,过滤 ①取少量滤液于试管中,滴入酚酞试液 ②取少量滤渣于试管中,加入盐酸 | ①滤液不变色 ②有气泡产生 | 氢氧化钙全部 变为碳酸钙 |

(4)原理与用途:①氢氧化钙俗称 ,(0.5分)农业上一般采用氢氧化钙改良
性土壤(选填“酸”或“碱”)。(0.5分)
②氢氧化钙变质是由于, (用化学方程式说明理由)
小华是个非常爱动脑的同学,做溶液的导电性实验时,小华观察得非常仔细,以下是他们小组观察、记录并思考的一些问题:
(1)电解水时,通常要加入少量氢氧化钠溶液或稀硫酸,目的是 。
(2)经过溶液的学习后,小华明白了不是所有的溶液都能导电的道理,下列物质加入水中充分振荡后能导电的是( )
| A.蔗糖 | B.植物油 | C.高锰酸钾 | D.碳酸钠 |
(4)若某氢氧化钠溶液中钠离子和水分子的个数比为1:20,则该溶液中溶质的质量分数为: 。(不要求计算过程)
(5)做氯化钠溶液的导电性实验时,小华不仅看到灯泡亮了,还观察到与电解水相似的现象:两根石墨电极上都出现了气泡。这激发了小华探究气泡成分的欲望。请你一起参与小华的探究活动吧!
【提出问题】氯化钠溶液通电时石墨电极上分别生成了什么气体?
【查阅资料】Cl2是黄绿色、有刺激性气味的有毒气体,常温下1体积水能溶解2体积Cl2。
【提出假设】假设1:电极上分别生成了氢气和氯气;
假设2:电极上分别生成了氧气和氯气;
假设3:电极上分别生成了氢气和氧气。以上假设的依据是 。
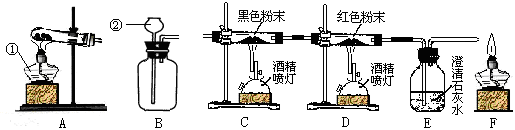
【设计实验】小红决定用电解水的装置重做氯化钠溶液的导电性实验。

【进行实验】用如图所示的实验分别收集氯化钠溶液通电
时两个电极上产生的气体。
【收集证据】观察气体颜色,刚燃着的木条检验收集到的无色气体,
发现氯化钠溶液在通电条件下产生了两种气体。
【实验分析】若一支试管中收集剑的气体为黄绿色,另一支试管中收集到的气体能支持燃烧,则假设 成立:若两支试管内收集到了两种不同的无色气体,则发生反应的化学方程式为 。
实验证明假设l成立,并且氯化钠溶液通电时还生成了氢氧化钠,请写出氯化钠溶液通电时发生反应的化学方程式_ ___。
【反思与评价】联想电解水的实验,你认为在电解水时 (填“可以”或“不可以”)加入少量的氯化钠溶液,原因是 。
假期,王霞同学在家中与妈妈做面包,发现妈妈揉面粉时在面粉中加入一种白色粉末,做出的面包疏松多孔,口感很好。她很感兴趣,想探究这种“神奇粉末”的成分。
【查阅资料】通过对市场上相关产品进行调查,王霞发现了如下图所示的三种商品,
王霞妈妈告诉她所用的白色粉末就是以上三种商品中的一种,发酵粉发酵过程会产生一种气体,你认为该气体是_________。
(1)【设计实验】王霞探究这种白色粉末的成分。
取少量白色粉末于试管中,加入适量蒸馏水,发现白色粉末溶解,无其他明显现象,则该白色粉末不是__________ (填商品名) ;另取少量白色粉末于试管
中,加入_______,有无色气体产生,王霞认为白色粉末是纯碱。
(2)【实验反思】小明同学认为王霞同学根据上面的实验现象,不能得出白色粉末是纯碱,为了得到鉴别纯碱和小苏打的正确方法,王霞继续查找资料,发现它们有下列的性质
| 性质 | 碳酸钠 | 碳酸氢钠 |
| 溶解性 | 20℃时溶解度21.6g,溶解 时放热 | 20℃时溶解度9.8g,溶解时 放热 |
| 加热 | 不分解 | 发生分解反应,分解产物为 碳酸钠、二氧化碳和水。 |
(3)在查找资料过程中,王霞同学还发现纯碱不是碱,是由于其水溶液显碱性而得名。现要验证纯碱溶液是否显碱性,把一小块试纸放在玻璃片上,用沾有待测溶液的
玻璃棒点在试纸上,观察颜色,与___ __对比,读数。