(11分)利用纯碱在实验室可以制取许多物质,某研究性学习小组对纯碱展开如下探究: Ⅰ.利用纯碱和稀盐酸制取二氧化碳
Ⅰ.利用纯碱和稀盐酸制取二氧化碳
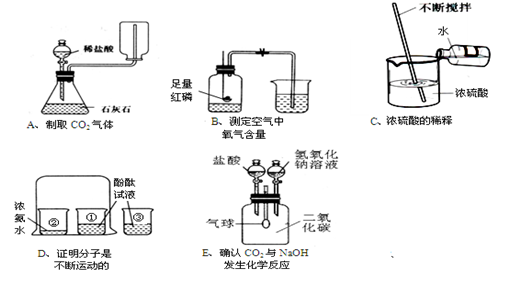
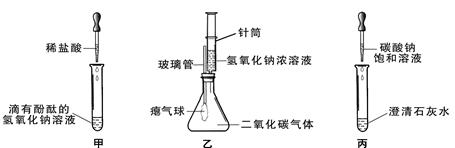
(1)写出右图装置B中标号仪器名称 ,用纯
碱和稀盐酸制取二氧化碳的反应方程式为 。
应该选用的发生装置为 ,用装置C收集二氧化
碳导气管需伸到集气瓶底部,目的 。
(2)有人认为用稀硫酸和纯碱制取二氧化碳,优于用稀
盐酸和纯碱制取二氧化碳,理由是 。
Ⅱ.利用纯碱和熟石灰制取烧碱溶液
步骤一:将纯碱溶于水,加入适量熟石灰;步骤二:过滤;步骤三:检验滤液中存在的溶质。
(3)步骤一中需要使用玻璃棒,其作用是 ,纯碱与熟石灰反应方程式为 。
(4)步骤二中过滤器中滤纸没有紧贴漏斗内壁的后果是 。
(5)小红按下表完成步骤三,请你将小红的实验设计补充完整。
| | 实验操作 | 实验现象 | 实验结论 |
| ① | 取少量滤液,滴入纯碱溶液 | 没有白色沉淀产生 | |
| ② | 另取少量滤液,滴入 ,静置。 | | 含有碳酸钠 和氢氧化钠 |

 这种产品可对车内及室内空气中的一氧化碳、甲醛等有害气体
这种产品可对车内及室内空气中的一氧化碳、甲醛等有害气体