(7分)小明在家中探究食用白醋的性质,选用了家庭生活中的下列常见物品:200ml的软透明塑料瓶、食品干燥剂、白醋、鸡蛋壳、紫罗兰花、锈铁钉、蒸馏水、纯碱、玻璃小杯。
【问 题】白醋是否具有酸类的性质?
【查阅资料】
(1)白醋为无色透明液体,其主要成分是醋酸,化学式可表示为HAc, Ac代表醋酸根;
(2)食品干燥剂的主要成分是氧化钙;
(3)紫罗兰花遇酸变为红色;
(4)醋酸盐中除银盐和汞盐外都易溶解于水。
【探究与验证】(请你帮助填写表中空白)
| 实验序号 | 实验操作 | 实验现象 | 实验结论 |
| 一 | 将白醋滴在紫罗兰花上 | 紫罗兰花变红 | 白醋的pH 7 |
| 二 | 将锈铁钉放在小玻璃杯中,加入白醋 | 刚开始时 ,一段时间后,有气泡冒出 | 1.白醋能与铁锈反应 2. |
| 三 | 向软塑料瓶中加入10ml白醋,将瓶捏扁,加入约5g鸡蛋壳,拧紧瓶盖 | 瓶中有气泡冒出,扁塑料瓶逐渐膨胀 | 白醋能与碳酸钙反应放出CO2 |
| 四 | 向白醋中加入纯碱 | 白醋中有 | 白醋能与碱反应 |
(1)小明将干燥剂袋口打开一段时间后,袋中的白色颗粒粘在了一起,请写出变化的化学方程式 。
(2)上面“实验结论”中,错误的是(填实验序号) 。
(3)上述实验三的现象还不足以得出表中所述的相应结论,为此还需要补充相应的实验,写出该实验发生反应的化学方程式 。
酒精灯灯焰分焰心、内焰和外焰三个部分。为探究灯焰温度,科研人员用特殊的测温装置进行实验,结果如下(探头位置是指测温探头离灯芯的垂直高度)。
| 火 焰 | 焰 心 | 内 焰 | 外 焰 | ||||
| 探头位置(cm) | 0.5 | 1.5 | 2.5 | 3.0 | 3.5 | 4.0 | 4.5 |
| 火焰温度(℃) | 537 | 670 | 775 | 806 | 801 | 750 | 667 |
| 平均温度(℃) | 603 | 794 | 708 | ||||
(2)灯焰焰心温度较低,其原因是_________________________。
(3)实验中,若燃着的酒精灯中酒精不足,现要添加酒精,采取的操作是:先__________,再向酒精灯中添加酒精。
已知在溶液中氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠。现实验室有一瓶失去标签但密封保存良好的白色粉末,可能是碳酸钠,也可能是氧化钙或氢氧化钙。为确定其组成,某同学设计了以下实验方案进行探究,请你按要求帮助完成探究活动。
(1)提出假设:假设①白色粉末是碳酸钠;假设②白色粉末是氧化钙;假设③白色粉
末是氢氧化钙。
| 设计的相关实验操作 | 实验中观察到的现象 | 假设是否成立 |
| 取一定量粉末加入稀盐酸 | 没有气体产生 | 假设① |
| 取一定量粉末溶于水 | 溶液浑浊且温度升高 | 假设② |
| 假设③ |
根据假设②的现象写出对应的化学方程式________________________________;
(3)实验后思考:假定这包白色粉末是混有少量氧化钙的碳酸钠粉末,将混合物溶于水可观察到的现象是_____________________________________________________;若将反应后的混合物进行固液分离,分离的方法是________;再将分离后的溶液蒸干,得到的固体物质是________、__________(填化学式)。
| 假设是否成立 |
| 否 |
| 是 |
| 否 |
(7分)牙膏是最常用的日用化学品之一,牙膏的成分有活性物质、摩擦剂、保持牙膏湿润的甘油等物质。
【查阅资料】①牙膏摩擦剂的主要成分有CaCO3、Al(OH)3、SiO2。
②SiO2不溶于水,也不与酸反应。
③维生素C的水溶液pH小于7,显酸性。
某品牌牙膏含有上述摩擦剂中的两种成分,为探究摩擦剂的组成,化学兴趣小组取适量该牙膏加水充分搅拌、静置、过滤、洗涤、干燥,得到该牙膏中的摩擦剂。
【提出猜想】猜想1:摩擦剂的成分为Al(OH)3和CaCO3。
猜想2:摩擦剂的成分为_______________。
猜想3:摩擦剂的成分为SiO2和Al(OH)3。
【设计实验】
| 实验步骤 | 预期实验现象 | 预期实验结论 |
| 取少量摩擦剂于试管中,加入足量的稀盐酸 | 若摩擦剂________________________。 | 则猜想1成立 |
| 若摩擦剂部分溶解,不产生气泡。 | 则猜想___成立 |
【实验反思】
(1)氢氧化铝与盐酸反应的化学方程式为 _ _。
(2)实验中选用稀盐酸而不选用稀硫酸的原因是_____________________________。
(3)根据实验结论,该品牌的牙膏中应该没有添加维生素C,理由是___________。
(7分)某同学进行试验探究时,欲配制10%的Ba(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2试剂。在室温下配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存在未溶物。为探究原因,该同学查得Ba(OH)2在20℃时的溶解度2.1 g。
(1)烧杯中未溶物仅为BaCO3,理由是(用化学方程式表示) 。
(2)假设试剂由大量Ba(OH)2和少量BaCO3组成,设计试验方案,进行成分检验,在答题卡上写出实验步骤、预期现象和结论。
限选试剂及仪器:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、氯化铜溶液、烧杯、试管、带塞导气管、滴管
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀。 | |
 步骤2:取适量滤液于试管中,滴加稀硫酸。 步骤2:取适量滤液于试管中,滴加稀硫酸。 | 有 ① 生成,说明有Ba2+ |
| 步骤3:取适量步骤1中的沉淀于是试管中,滴加稀盐酸,用带塞导气管塞紧试管,把导气管插入装有澄清石灰水的烧杯中。 | 试管中有 ②生成,烧杯中 ③ ,结合步骤2说明沉淀是BaCO3。 |
| 步骤4:取适量滤液于试管中, ④ 。 | 试管中有蓝色沉淀生成,说明有大量的OH—,综合上面步骤可知试剂由大量Ba(OH)2和少量BaCO3组成,假设成立。 |
五、计算与分析题(共2小题,共10分)
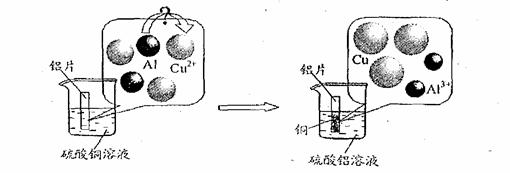
目前已制得的纯金属只有90余种,但由这些纯金属按一定组成和质量比制得的合金已达几千种。由于合金更容易适合不同的用途,因此被大量应用于日常生活、工农业及科学研究中。结合所学知识,完成27、28题。
阿明同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题.她设计并完成了下表所示的探究实验:
| | 实验操作 | 实验现象 | 实验结论或总结 | |
| 结论 | 总结 | |||
| 实验一 | 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 | 有极少气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是分解速率 填______________。 (“较快”或“较慢”) | 二氧化锰是过氧化氢分解的催化剂 |
| 实验二 | 向盛水的试管中加入二氧化锰,伸入带火星的木条 | 没有明显现象 | | |
| 实验三 | 取5mL5%的过氧化氢溶液于试管中, 伸入带火星的木条 | 有大量气泡产生, | 二氧化锰能加快过氧化氢的分解反应的化学方程式为: | |
(2)在小丽的探究实验中,“实验一”和“实验二”起的作用是
(3)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明.
第一方面的实验操作中包含了两次称量,其目的是:
第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验.接下来的实验操作、现象和结论是: , ,