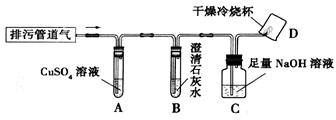
(11分)实验室有一瓶保管不当的试剂,其残缺的标签中只剩下“Na ”和“10%”字样。已知它是无色液体,是初中化学常用的试剂。小强和小华同学很感兴趣,决定对其成分进行探究:
【提出问题】这瓶试剂可能是什么溶液呢?
【查阅资料】Ⅰ.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3。
Ⅱ. Na2CO3和NaHCO3溶液都呈碱性,NaCl溶液呈中性。
Ⅲ.测定室温(20℃)时,四种物质的溶解度的数据如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
【作出猜想】①可能是 溶液;②可能是Na2CO3溶液;③可能是NaCl。
【设计并实验】(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,这瓶试剂不可能是 。
(2)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加 | 产生大量的气泡 | 猜想②正确。相关的化学方程式 |
| 把产生的气体通入 | | 相关的化学方程式 |
溶液。
(14分)某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究。
【产品原理】
该厂采用“侯氏制碱法”生产化工产品——纯碱(Na2CO3)和化肥NH4Cl。
生产原理是:将NH3和CO2通入饱和食盐水中得到NaHCO3晶体和NH4Cl溶液,反应的化学方程式为: ;后分离出NaHCO3,加热制得纯碱。
【生产流程】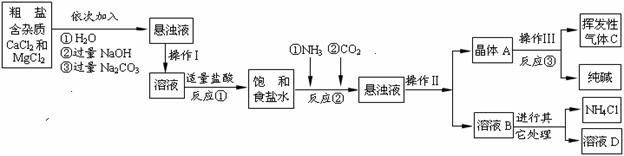
|
⑵已知20℃时有关物质的溶解度如下(气体指1体积水中能溶解的气体体积)
| 物质 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| 溶解度 | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
⑴操作Ⅰ、Ⅱ中,相同操作的名称为 。反应①中发生了两个反应,写出其中一个化学方程式: ,反应①加适量的盐酸,适量是指 。
⑵检验挥发性气体C的方法 。
⑶上述生产流程中可循环使用的是 (填序号)。
A.挥发性气体C B.溶液D C.氢氧化镁 D.化肥NH4Cl
【组成确定】
⑴称取一定质量的纯碱样品,经多次充分加热后,再称重,质量无变化;
⑵另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀。由上述实验可确定纯碱样品含有杂质 (写化学式)。
【含量测定】
| | 实验一 | 实验二 | 实验三 | 实验四 |
| 固体混合物溶液质量 | 100g | 100g | 100g | 100g |
| 加入CaCl2溶液质量 | 10g | 20g | 30g | 40g |
| 生成的沉淀的质量 | 4g | m | 10g | 10g |
称取该纯碱样品44 g固体混合物,加水配成400g溶液,平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见表:
请分析表中数据回答并计算:
⑴m= g;
⑵在实验三中,完全反应后所得溶液中溶质氯化钠的质量分数是多少?(要求写计算过程,结果保留0.1%)
【总结反思】
请通过计算并结合下表判断此纯碱样品等级为 品,在上述纯碱含量测定中,将CaCl2溶液改为BaCl2溶液,测定误差会减小。
(6分)以下是某研究小组探究影响反应速率部分因素的相关实验数据。
| 实验序号 | H2O2溶 液浓度% | H2O2溶液体积/mL | 温度℃ | MnO2的用量/g | 收集氧气的体积/mL | 反应所需 的时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 15 | 1 | 20 | 0 | 4 | 96.50 |
| ④ | 30 | 5 | 35 | 0 | 2 | 49.21 |
| ⑤ | 30 | 5 | 55 | 0 | 2 | 10.76 |
(1)通过实验①和②对比可知,化学反应速率与 有关;
(2)从实验 和 对比可知,化学反应速率与温度的关系是: ;
(3)通过实验②和③比较可知,使用 对化学反应速率影响很大。
(4)用一定量15%的过氧化氢溶液制氧气,为了减缓反应速率,可加适量的水稀释,产生
氧气的总重量 (选填“减小”或“不变”或“增大”)。
(10分)某学习小组在探究CO2与NaOH溶液反应的实验中,先用铝制易拉罐收集满一罐CO2气体,然后迅速向其中加入一定量的NaOH浓溶液,立即将易拉罐口封闭(不漏气),轻轻摇动易拉罐,发现易拉罐很快变瘪,但过一段时间后,易拉罐又重新鼓起来(反应过程中温度的变化忽略不计)。
【提出问题】易拉罐为什么先瘪后鼓?
【分析猜想】易拉罐开始时变瘪的原因是____________________________________(用化学方程式表示),易拉罐重新鼓起的原因是易拉罐中又生成了气体A,其成分极有可能是CO2或 H2。
【查阅资料】①Na2CO3具有较强的热稳定性,只有在高温条件下才会分解;
②铝单质比较容易被酸、碱腐蚀。
【设计方案并进行实验】
为了检验铝制易拉罐中重新生成的气体成分,小组又进行如下实验,并记录了相应的实验现象:
| 实验步骤 | 实验现象 | 实验结论 |
| ①将易拉罐口打开,迅速用燃着的木条伸入罐口。 | 发出“噗”的一声,产生淡蓝色火焰,片刻后熄灭。 | 说明罐中重新生成的气体A是________。 |
| ②取少量铝片于试管中,先加入适量的水,片刻后再加入少量的氢氧化钠溶液。 | 先加水,没有明显变化,后加入氢氧化钠溶液后产生无色无味的气体。 | 说明铝是否与水直接反应:______(填 “是”或“否”),铝能够与_______溶液反应。 |
| ③取少量易拉罐中反应后的溶液于试管中,加入过量的稀盐酸。 | 产生了无色无味气体,该气体能使澄清石灰水变浑浊。 | 说明原CO2气体被NaOH溶液吸收。 |
②铝制易拉罐重新鼓起的原因是铝与NaOH溶液反应产生了气体。
【反思评价】小组根据实验探究获得一条对金属铝化学性质的新认识:____________________
某化学兴趣小组的同学在课外读物中看到:“通常CO2可做灭火剂,但有些物质(如Na)着火,不能用CO2熄灭。”他们决定探究CO2与 Na反应的产物。
⑴提出猜想:CO2与 Na反应可能生成四种物质:C、CO、Na2O、Na2CO3。
⑵查阅资料:
①Na是非常活泼的金属,在常温下能与O2、H2O等物质反应。
②碱性的Na2CO3溶液与中性的CaCl2溶液能发生复分解反应;
③Na2O是白色固体,与H2O反应生成NaOH;
④向氯化钯(PdCl2)溶液中通入CO,产生黑色沉淀。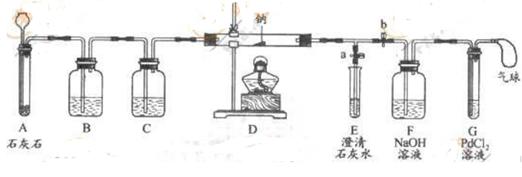
⑶实验过程:同学们在老师的指导下设计了如图所示的装置(夹持仪器已略去)
①实验记录:
| 序号 | 实验操作 | 主要实验现象 | 试验结论及解释 |
| Ⅰ | 打开a,关闭b,由长颈漏斗向A中注入稀盐酸 | A中产生大量气泡,E中出现浑浊 | E中反应的化学方程式为 |
| Ⅱ | 当E中出现浑浊时,打开b,关闭a,点燃酒精灯 | D中的Na剧烈燃烧,产生白烟,内壁附有黑色、白色固体;G中产生黑色沉淀 | 反应的产物中一定有 和 |
| Ⅲ | 将D中白色固体加入试管中,加水溶解,再加入澄清石灰水 | 产生白色沉淀 | 反应的产物中还有 |
Ⅰ.实验记录Ⅱ中,E中出现浑浊后埔再点燃酒精灯的目的是
Ⅱ.若无装置C,对实验有影响的物质是 。
Ⅲ.检验第四种物质是否存在的实验方案:将D中白色固体加入试管中,
。
(15分)某同学针对石蜡燃烧开展如下延伸探究,请你帮助解决探究过程的相关问题:
【提出问题】石蜡中除含碳、氢元素外,是否还含有氧元素?
【实验设计】根据质量守恒定律,该同学用精制石蜡、棉线烛芯做成蜡烛,设计了如下实验(其中浓硫酸、无水硫酸铜均易吸收水分,药品用量保证充足,部分固定装置省略)。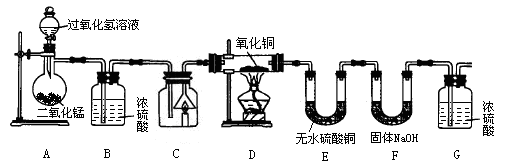
【操作原理】
(1)请写出A装置(含导气管)气密性的检查方法: 。装置A中发生反应的化学方程式是 。
(2)装置B的作用是 ;装置D的作用是 。
(3)装置F发生反应的化学方程式是 。
(4)为达到实验目的,反应前、后必须称量 (填装置序号)装置中的药品质量。
【数据处理】
(5)该同学在老师帮助下,经过一些补充实验和误差处理后得出了如下数据,请你帮助完成数据分析及结论部分。
| 实验事实 | 数据分析及结论 |
| 2.12 g石蜡完全燃烧,得到6.6g CO2和2.88g H2O | 写出计算过程: 结论: 。 |
(6)根据该学生设计的实验,你认为造成误差的原因是 (填写一条)。
(7)针对你提出的误差原因,提出减少误差的实验或改进措施: 。