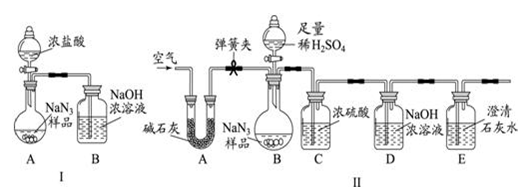
三位同学用下图所示装置做一氧化碳还原氧化铁的实验。请帮他们写出一氧化碳还原氧化铁的化学方程式 。当观察到玻璃管A中的粉末由红色逐渐变为黑色时,停止加热,继续通一氧化碳,冷却到室温,停止通气,同时观察到澄清的石灰水变浑浊。
用一氧化碳还原氧化铁的实验装置
小明认为:依据上述实验现象可以判断出生成的黑色固体为金属铁。
小红认为:仅从上述实验现象,不足以证明生成的黑色固体为金属铁,她增加了一个实验:用磁铁靠近生成的黑色固体,看到有黑色固体被磁铁吸引。于是得出生成的黑色固体为金属铁的结论。
小光通过查询有关资料得知:
(1)一氧化碳与氧化铁在加热条件下可能会生成四氧化三铁这种物质。
(2)四氧化三铁为黑色固体,有强磁性,也能够被磁铁吸引。
因此,小光认为小明和小红的结论都不能成立,你是否同意他的说法? ,
请具体说明你的理由 。
小光想通过实验检验生成的黑色固体是否含有金属铁。请你帮他完成实验并填写下表。
| 实 验 步 骤 | 实 验 现 象 | 实 验 结 论 |
| 取少量黑色固体于试管中,向其中滴加适量稀盐酸 | ① ②若没有气泡产生 | ①则黑色固体中含金属铁 ② |
请帮小光写出铁与硫酸铜溶液反应的化学方程式 。
假期,王霞同学在家中与妈妈做面包,发现妈妈揉面粉时在面粉中加入一种白色粉末,做出的面包疏松多孔,口感很好。她很感兴趣,想探究这种“神奇粉末”的成分。
【查阅资料】通过对市场上相关产品进行调查,王霞发现了如下图所示的三种商品,
其中,发酵粉与水混合后,产生大量气体,你认为该气体是 。王霞妈妈告诉她所用的白色粉末就是以上三种商品中的一种。
(1)【设计实验】王霞探究这种白色粉末的成分。
取少量白色粉末于试管中,加入适量蒸馏水,发现白色粉末溶解,无其他明显现象,实验结论是 ;另取少量白色粉末于试管中,加入 ,有无色气体产生,王霞认为白色粉末是纯碱。
(2)【实验反思】小明同学认为王霞同学根据上面的实验现象,不能得出白色粉末是纯碱,你若认为小明说法有道理,请用化学方程式解释不能得出结沦的原因 。为了得到鉴别纯碱和小苏打的正确方法,王霞继续查找资料,发现它们有下列的性质
| 性质 | 碳酸钠 | 碳酸氢钠 |
| 溶解性 | 20℃时溶解度21.6g,溶解时放热 | 20℃时溶解度9.8g,溶解时放热 |
| 加热 | 不分解 | 发生分解反应,分解产物为碳酸钠、二氧化碳和水。 |
(3)在查找资料过程中,王霞同学还发现纯碱不是碱,是由于其水溶液显碱性而得名。现要验证纯碱溶液是否显碱性,请写出用pH试纸来测其pH值的操作过程 。
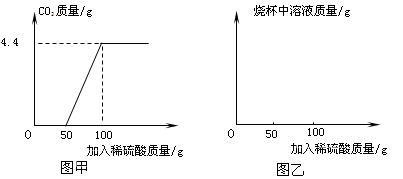
(5分)化学兴趣小组同学按下图一实验时,发现有气泡产生,于是对这异常现象进行了探究。
(1)对气体成分的探究:加热MnO2样品,将燃着的木条伸入管口,木条熄灭,将气体通入澄清石灰水,变浑浊,由此知产生的气体是 ① 。
(2)对气体来源的探究:
①假设一:甲同学认为该气体来源于试管中的空气,请你设计实验证明该假设不成立。
| 实验步骤及现象 | 结论 |
| ② | 假设不成立 |
③丙同学认为,乙同学得出的结论不严密。图二中通入的是空气,虽然用A除去了空气中可能含有的该气体,但在B处有可能发生反应 ④ (写出方程式)生成该气体,所以,应该把空气换成 ⑤ ,这样乙的推断就严密了。
(9分)某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验。
I、实验方案
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,测得的pH逐渐变小直到pH小于7,则证明NaOH溶液与稀盐酸发生了化学反应。
⑴反应后,所得溶液显 性(填“酸”、“碱”或“中”)
⑵用pH试纸测定NaOH溶液pH时,正确的操作是:
。
⑶简述强调“测得的pH小于7”的理由:
______________________________________________________________________________。
方案二:化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生。如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应。
该组同学将不同浓度的盐酸和NaOH溶液各10 克混合,用温度计测定室温下混合前后温度的变化,并记录了每次混合前后温度的升高值△t(如下表)。
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65﹪ | 2.00﹪ | 3.5 |
| 2 | 3.65﹪ | 4.00﹪ | x |
| 3 | 7.30﹪ | 8.00﹪ | 14 |
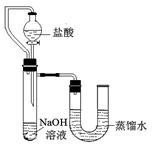
⑸某同学在没使用温度计的情况下,通过下图所示装置完成了实验。则该同学根据实验现象:
,判断NaOH溶液与稀盐酸发生了中和反应。
II、实验中的意外情况
在实验过程中,他们发现盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末。他们依据所学的化学知识,对这种白色粉末的成分作了如下猜想:①可能是NaOH;②可能是Na2CO3;③可能是NaOH和Na2CO3。
⑹小明同学取白色粉末少许,溶于水后,先向溶液中加入足量的 溶液,看到白色沉淀产生,然后向上层清液中加入酚酞试液,看到溶液呈红色,验证了猜想③是正确的。
⑺为了进一步研究,三位同学取了10.0g上述样品,利用电子天平共同做了下图所示的实验。

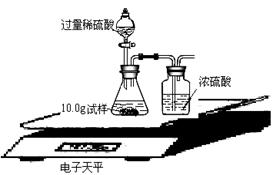
实验数据记录如下:
| 称 量 项 目 | 称 量 时间 | 质量(g) |
| 试样 | | 10.00 |
| 装置+稀硫酸质量 | | 241.20 |
| 装置+稀硫酸质量+试样 | 反应开始后15秒 | 249.20 |
| 装置+稀硫酸质量+试样 | 反应开始后35秒 | 247.00 |
| 装置+稀硫酸质量+试样 | 反应开始后55秒 | 247.00 |
(8)有同学提出按上述实验所测得试样中Na2CO3质量分数会偏小,该同学的理由是(实验操作均正确): 。
在日常生活中,有这样的说法,“肥皂水是碱性的,洗衣粉溶液是酸性的”。这种说法正确吗?肥皂和洗衣粉混用会降低去污效果吗?某科学兴趣小组对此进行了探究,实验过程如下:
①取三个塑料杯,分别编为甲、乙、丙,在甲杯中加入5克洗衣粉、乙杯中加入5克肥皂、丙杯中加入2.5克洗衣粉和2.5克肥皂混合。
②在三个塑料杯中,分别加入相同温度、相同质量的水,充分搅拌使之完全溶解,并测出溶液pH。
③在相同温度下,将三块大小、油污程度均相同的白棉布分别放入三杯溶液中浸泡10分钟后,取出观察,实验结果记录如下:
| | 甲 | 乙 | 丙 |
| 洗涤前洗涤剂溶液pH | 10 | 8 | 9 |
| 去污效果 | 基本去除油污 | 基本去除油污 | 基本去除油污 |
| | 甲 | 乙 | 丙 |
| 洗涤前洗涤剂溶液pH | 8 | 9 | 9 |
| 去污效果 | 完全去除油污 | 完全去除油污 | 完全去除油污 |
(1)“肥皂水是碱性的,洗衣粉溶液是酸性的”,这种说法正确吗? (选填“正确”或“不正确”)。
(2)将肥皂和洗衣粉混合使用会降低去污效果吗? (选填“会”或“不会”)。
(3)为什么要换另一种品牌洗衣粉和肥皂重复同样的实验?
钛(Ti)是一种重要的航天金属材料.某学习小组为了探究Ti、 Al 、 Cu的金属活动性:
[提出假设] a. Ti金属活动性比Al强 b. Al金属活动性比Cu强
[查阅资料] Ti能与盐酸反应。
[实验设计] 同温下,取大小相同的这三种金属薄片,分别投入等体积等浓度的足量的盐酸中反应,观察现象。
[操作分析] 三种金属加入盐酸前都先用砂布将表面擦光亮,其目的是
A 除去氧化膜,利于直接反应 B 使表面光亮,易观察现象
C 使反应金属温度相同,易反应
[实验现象]
| 金属 | Ti | Al | Cu |
| 与盐酸反应 | 反应缓慢 | 反应剧烈 | 无明显现象 |
(2)三种金属的金属活动性由强至弱的顺序为 。
[结论应用] 能否用铝制容器来盛放波尔多液(含硫酸铜) 。(填“能”或“不能”)
某活动小组的同学对碳酸钠与稀盐酸反应进行了下列探究:
【探究一】向放有一支燃着的蜡烛的烧杯中加适量碳酸钠和盐酸(如图所示):
(1)蜡烛燃烧变化的现象是: 。
(2)根据该实验现象推测碳酸钠与盐酸反应产生的气体可用于 (写出用途)。
【探究二】利用碳酸钠与盐酸的反应,可否用于验证质量守恒定律进行了探究,实验如下,如图所示,

在(吸滤)瓶中加入适量的碳酸钠粉末,在小试管中加入盐酸。将小试管放入吸滤瓶中,并用止水夹夹住支管处的橡皮管。称量整个装置的质量,记录读数。将吸滤瓶倾斜,使小试管中的盐酸倾倒入瓶中,与碳酸钠粉末反应。可观察到如图二所示的现象。再次称量整个装置的质量,记录读数。
两次读数 (填“是”或“否”)相等。理由是 。
【探究三】碳酸钠与盐酸反应后剩余溶液的成分探究(假设二氧化碳已完全放出,杂质溶于水,不参加反应且呈中性)。甲、乙两同学分析认为剩余溶液中一定含有氯化钠,可能有盐酸或碳酸钠。为验证是否含有盐酸,他们采用了不同方法进行实验,得到了相同的结论。
查找资料:氯化钠溶液呈中性
| | 实验操作 | 实验现象 | 结论 |
| 甲 | 取样于试管中,滴加 试液 | 试液变红 | 有盐酸 |
| 乙 | 取样于试管中,逐滴滴加碳酸钠溶液 | |
(1)产生的二氧化碳的质量为 g。
(2)纯碱样品中碳酸钠的质量(写出计算过程)。