下列事实不能用同一原理进行解释的是
| A.C和CO都能跟灼热的CuO反应 |
| B.实验室收集C02和02都能用向上排空气法 |
| C.碳酸饮料和白醋都能使紫色石蕊试液变红 |
| D.在滴有酚酞的NaOH溶液中滴加盐酸和投入活性炭都能使溶液褪色 |
下列除去杂质的方法中,错误的是( )
| 物质 | 杂质 | 除杂质的方法 |
| A.CaCl2溶液 | HCl | 过量CaCO3、过滤 |
| B.NaOH溶液 | Ca(OH)2 | 过量Na2CO3溶液过滤 |
| C.FeCl2溶液 | CuCl2 | 过量铁粉、过滤 |
| D.CH4 | H2O | 通过盛浓硫酸的洗气瓶 |
下图为常见的实验装置,下列实验设计能达到实验目的的是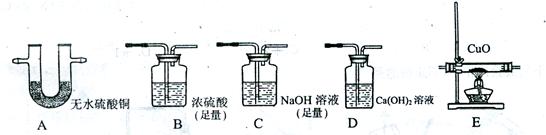
| A.若要将含水蒸气的氢气干燥后还原氧化铜,则该气体先要通过装置B ’ |
| B.若要验证混合气体中有H2和H2O,则装置的连接顺序应为AEA |
| C.若要验证混合气体中有H2、CO和H2O,则装置的连接顺序应为ABEDA |
| D.若要验证混合气体中有CO2、CO、H2,则装置的连接顺序应为DCBEAD |
我市某电镀厂为减少水污染及节约成本,从含有CuSO4、ZnSO4、FeSO4的废水中回收重要原料硫酸锌和有关金属,实验过程如下图: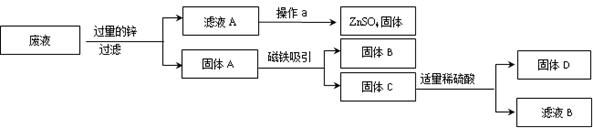
结合以上提纯过程,下列分析完全正确的是
| | 固体A | 操作a | 固体C | 滤液B(溶质) |
| A. | Cu、Fe | 过滤 | Cu | ZnSO4、H2SO4 |
| B. | Cu、Fe、Zn | 蒸发 | Cu | ZnSO4、H2SO4 |
| C. | Cu、Fe、Zn | 蒸发 | Cu、Zn | ZnSO4 |
| D. | Cu、Fe | 加入金属锌 | Cu、Zn | ZnSO4、FeSO4 |
有一包固体可能含有CaCl2、Na2SO4、Na2CO3、KNO3中的一种或几种,现对其进行如下实验:①取少量固体于试管中,加适量蒸馏水,固体完全溶解形成无色透明溶液;②取少量上述溶液,加过量稀盐酸,有气泡产生; ③取②所得溶液少量,滴加BaCl2溶液,产生白色沉淀。分析以上实验现象,对原固体组成的推断正确的是 ( )
| A.肯定有Na2CO3,无CaCl2 |
| B.肯定有Na2CO3、Na2SO4,无CaCl2 |
| C.肯定有Na2CO3、Na2SO4,可能有KNO3、CaCl2 |
| D.肯定有Na2SO4,可能有KNO3、CaCl2 |
下列物质的鉴别方法错误的是
| A.用水鉴别硝酸铵固体和氢氧化钠固体 | B.用带火星的木条鉴别空气和氧气 |
| C.用灼烧法鉴别棉纤维和羊毛纤维 | D.用酚酞溶液鉴别稀盐酸和稀硫酸 |
固体物质A与盐酸反应生成溶液B,B与氢氧化钾反应得到沉淀C,C加热又转化为A,则A不可能是 (提示:不溶性碱受热分解生成金属氧化物和水)( )
| A.氧化钠 | B.氧化铜 | C.氧化镁 | D.氧化铁 |
厨房里有自来水、白酒、精盐、碳酸钠粉末、食醋、蜡烛、火柴、玻璃杯等用品,利用厨房的这些用品无法完成的小实验是( )
| A.鉴别自来水和白酒 | B.鉴别精盐和碳酸钠粉末 |
| C.测试食醋的pH | D.验证二氧化碳可以灭火 |
除去CO2中混有的少量CO杂质可采用的适宜方法是( )
| A.点燃混合气体 | B.将混合气体通过石灰水 |
| C.将混合气体通过灼热的CuO | D.将混合气体通入水中 |