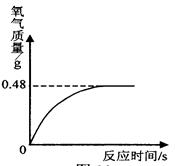
某学校的学习小组对当地的石灰石矿区进行调查,测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品16g,把80g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的等杂质不溶于水也不与稀盐酸反应)。Ca CO3十2HCl= CaC12十H2O十C02↑
请计算:
| 序号 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
| 第1次 | 20 | 12 |
| 第2次 | 20 | 8 |
| 第3次 | 20 | 4.8 |
| 第4次 | 20 | n |
(2)石灰石中碳酸钙的质量分数为 。(6分)(写出计算过程)。
(3)反应前盐酸的质量分数?
“黄铜”即铜锌合金,古代称为“俞石”。由于外观酷似黄金,常被不法商贩冒充黄金出售。某实验小组为了辨别真伪,用该合金与稀盐酸反应,将三次实验所得相关的数据记录如下:
| 物质质量 | 第1次 | 第2次 | 第3次 |
| 所取合金的质量/g | 25 | 25 | 50 |
| 所用稀盐酸的质量/g | 120 | 160 | 100 |
| 充分反应后,剩余物总质量/g | 144.6 | 184.6 | 149.6 |
(2)计算铜锌合金中的铜的质量分数;
(3)计算恰好完全反应后所得溶液中溶质的质量分数(得数保留一位小数)。
(10分)某化学兴趣小组为测定大理石中碳酸钙的含量,将过量的稀盐酸加入到20 g大理石中(其它成分不与盐酸反应),把产生的CO2气体用足量的NaOH溶液吸收,同时测量2分钟内NaOH溶液增加的质量,结果如下表所示:
| 时间/s | O | 20 | 40 | 60 | 80 | 100 | 120 |
| 增加的质量/g | O | 3.O | 5.O | 6.O | 6.6 | 6.6 | 6.6 |
试回答下列问题:
(1)请在右边的坐标纸上,以反应时间为横坐标,以产生CO2气体的质量为纵坐标,画出能够表明产生气体的质量随时间变化规律的关系曲线;
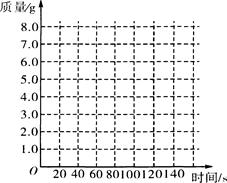
(2)从表中可以看出,20 g大理石样品与盐酸反应生成的CO2质量最多是 g;
(3)计算大理石样品中碳酸钙的质量分数。
锌是人体健康所必需的元素,锌缺乏容易造成发育障碍,易患异食癖等病症,使人体免疫力功能低下。市售的葡萄糖酸锌口服液对治疗锌缺乏症具有较好的疗效。下图是某品牌葡萄糖酸锌口服液的标签,请根据标签信息回答:
| ××牌口服液 主要成份:葡萄糖酸锌 化学式:C12H22O14Zn 每支口服液含葡萄糖酸锌45.5mg ××制药厂 |
(2)葡萄糖酸锌中锌元素的质量分数为 。(精确到0.01%)
(3)某患者除正常饮食吸收锌元素外,还需服用该品牌葡萄糖酸锌口服液。若治疗一个疗程需要补充104mg锌元素,而这些锌有75%来自于该口服液,则患者共需要服用 支葡萄糖酸锌口服液?