为了对海水中的氯化物(假设以NaCl计算)进行成分分析,甲、乙、丙三位同学分别进行实验数据如下,请仔细观察分析,回答下列问题:
| | 甲 | 乙 | 丙 |
| 所取海水样品的质量 /g | 100 | 50 | 50 |
| 加入AgNO3溶液的质量 /g | 50 | 50 | 75 |
| 反应后所得的沉淀物的质量 /g | 1.435 | 1.435 | 1.435 |
(2)请计算海水中的氯化物(以氯化钠计算)的质量分数是多少?
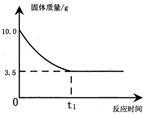
(5分)实验时中有一瓶存放时间过长的NaOH药品,其中一部分已转化为Na2CO3取10克该药品放入烧杯中,加154克水配成溶液,将400克一定溶质质量分数的Ca(OH)2 溶液分四次加入该烧杯中,充分反应后,测得生成沉淀质量的数据记录如下表:
| 次数 | 1 | 2 | 3 | 4 |
| 加入Ca(OH)2溶液的质量/克 | 100 | 100 | 100 | 100 |
| 烧杯中生成沉淀的质量/克 | 1 | m | 3 | 3 |
(2)求10克该药品Na2CO3中的质量
(3)第三次加入Ca(OH)2溶液充分反应后,所得溶液中溶质质量分数是多少?
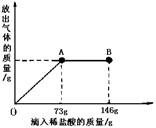
(6分)某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成,取四份样品分别加稀硫酸反应,其实验数据记录如下表。
| 样品 | 第1份 | 第2份 | 第3份 | 第4份 |
| 取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
| 取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
| 产生气体质量(g) | 0.4 | 0.8 | 1.0 | 1.0 |
(1)经分析,在第1份样品测得的数据中, (填物质)完全反应了。
(2)列式计算黄铜屑样品中的锌的质量分数和所用稀硫酸中溶质的质量分数。