(2012·德阳)将Na2SO4和NaOH的混合物10g投入到200g溶质质量分数为4.9%的H2SO4溶液中恰好完全反应。请计算:
(1)10g混合物中NaOH的质量;
(2)最后所得溶液中溶质的质量。
(7分)某同学为了测定NaCl和MgCl2固体混合物中MgCl2的质量分数,进行如下实验:将80g固体混合物溶于水配成溶液,平均分成四份,分别加入相同质量分数的NaOH溶液,获得如下实验数据:
| 实验次数 | 一 | 二 | 三 | 四 |
| 固体混合物的质量(g) | 20 | 20 | 20 | 20 |
| 加入NaOH溶液的质量(g) | 20 | 40 | 60 | 80 |
| 生成沉淀的质量(g) | 2.9 | m | 8.7 | 8.7 |
A.表中m的值为 ;(2分)
B.原固体混合物中MgCl2的质量分数是多少?(5分)(要求写出计算过程)
(6分)“黄铜”即铜锌合金,古代称为“俞石”。由于外观酷似黄金,常被不法商贩冒充黄金出售。某实验小组为了辨别其真伪,用该合金与稀硫酸反应,进行了三次实验,所得相关的实验数据记录如下:
| | 第一次 | 第二次 | 第三次 |
| 所取合金的质量/g | 25 | 25 | 50 |
| 所用稀硫酸的质量/g | 120 | 160 | 100 |
| 充分反应后,剩余物总之量/g | 144.6 | 184.6 | 149.6 |
(2)计算铜锌合金中的铜的质量分数。
(3)计算恰好完全反应后所得溶液中的溶质的质量分数。
(6分)(2012?巴中)某化学兴趣小组同学为测定锌铜合金中锌的质量分数,称取8.0克合金样品,将60.0克稀硫酸分6次加入样品中,充分反应后过滤、洗涤、干燥、称量.得到实验数据如下.
| 稀H2SO4用量 | 剩余固体质量 |
| 第一次加入10.0克 | m |
| 第二次加入10.0克 | 5.4克 |
| 第三次加入10.0克 | 4.1克 |
| 第四次加入10.0克 | 2.8克 |
| 第五次加入10.0克 | 1.6克 |
| 第六次加入10.0克 | 1.6克 |
(2)该锌铜合金锌的质量分数为 _________ .
(3)计算所用稀H2SO4中溶质的质量分数.(请写出计算过程,结果精确到0.1%)
为测定某地石灰石样品中碳酸钙的质量分数,进行以下实验;向装有10.0g石灰石样品的烧杯中,加入47.2g稀盐酸,恰好完全反应,烧杯中剩余物质的总质量随时间变化关系如下表:(石灰石中的杂质不参加反应且难溶于水)
| 时间/min | t1 | t2 | t3 | t4 | t5 | t6 |
| 烧杯中剩余物质的总质量/g | 56.7 | 56.2 | 55.7 | 55.2 | 55.0 | 55.0 |
(2)样品中碳酸钙的质量分数;
(3)将反应后烧杯中的剩余物质进行过滤,再向滤液中加入多少克水可以得到5%的氯化钙溶液?
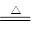 Na2CO3 + H2O + CO2↑ ,碳酸钠受热不分解),完全分解生成二氧化碳气体0.22g。求:样品中碳酸钠的质量分数。
Na2CO3 + H2O + CO2↑ ,碳酸钠受热不分解),完全分解生成二氧化碳气体0.22g。求:样品中碳酸钠的质量分数。