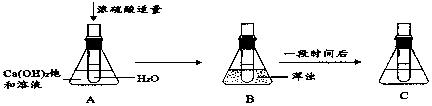
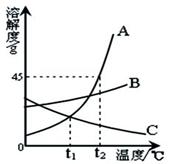
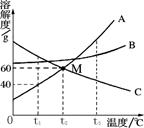
溶液在生产和生活中有重要意义。
(1)某兴趣小组为了研究物质的溶解和结晶,做了如下所述过程的实验: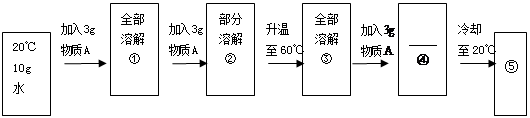
小资料:氯化钠和硝酸钾的溶解度数值:
| 项目 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ |
| NaCl | 35.8g | 36.0g | 36.3g | 36.6g | 37.0g | 37.3g | 37.8g |
| KNO3 | 20.9g | 31.6g | 45.8g | 63.9g | 85.5g | 110g | 138g |
①物质A是 (填“氯化钠”或“硝酸钾”)
②状态“④”时,物质A 溶解(填“部分”或“全部”)
③上述实验过程中所得溶液达到饱和的是_______(填数字序号,下同);溶质质量分数最大的是 。
下表是KNO3、NaCl在不同温度下的溶解度(单位:g):
| 温度(℃) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| KNO3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 |
| NaCl | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 |
(2)20℃时,食盐饱和溶液中溶质的质量分数是 。(保留一位小数)
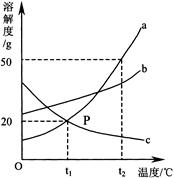
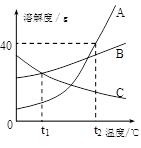
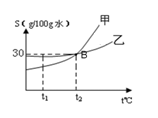
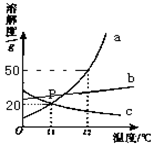
(3)用上表数据来画溶解度曲线,两种物质的曲线相交时的温度范围应是 。(填字母序号)
A.10~20℃ B.20~30℃ C.30~40℃ D.40~50℃
(4)70℃时,将138gKNO3、37gNaCl分别溶解在各装有100g水的两个烧杯中,其中能形成饱和溶液的是 ;若从70℃降到20℃后,下列说法中正确的是 (填字母序号)。
A.KNO3析出,NaCl不析出
B.其溶剂的质量不变
C.KNO3和NaCl的质量分数都降低
D.KNO3的质量分数降低,NaCl的质量分数不变