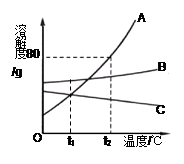
甲、乙、两种不含结晶水的固体物质的溶解度曲线如图所示.根据图示判断,下列说法中,不正确的是( )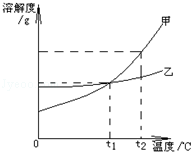
| A.甲、乙两种物质的溶解度都随温度的升高而增大 |
| B.在t1时,甲、乙两物质饱和溶液溶质的质量分数相等 |
| C.将t1时甲的饱和溶液升温(溶剂不蒸发),溶液浓度增大 |
| D.当甲含有少量乙时,可用冷却热饱和溶液的方法提纯甲 |
A图是物质M和N的溶解度曲线.B图中甲、乙试管分别盛有M、N的饱和溶液,试管底均有未溶解的M、N固体.向烧杯中加入一种物质后,甲中的固体减少,乙中的固体增加,则加入的物质不可能是( )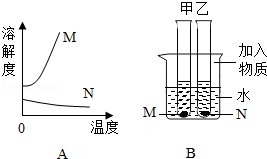
| A.浓硫酸 | B.硝酸铵固体 | C.氧化钙 | D.氢氧化钠固体 |
如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法错误的是( )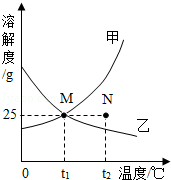
| A.甲物质的溶解度随温度的升高而增大 |
| B.在t1℃时,甲、乙两物质的溶解度相等 |
| C.在t2℃时,N点表示甲物质的不饱和溶液 |
| D.在t1℃时,100g乙物质的饱和溶液中溶质的质量是25g |
下列各项中,前者一定大于后者的是( )
| A.20℃时KNO3的溶解度、80℃时KNO3的溶解度 |
| B.30℃时:NaCl不饱和溶液的质量分数、NaCl饱和溶液的质量分数 |
| C.10g镁与足量盐酸反应生成H2的质量、10g铝与足量盐酸反应生成H2的质量 |
| D.NaOH溶于水后溶液的温度、NH4NO3溶于水后溶液的温度 |
据《说文解字》记载,我们的祖先在神农氏时代就已经开始利用海水晒盐。海水晒盐的原理是
| A.风吹日晒使溶液由饱和变为不饱和 |
| B.风吹日晒使氯化钠的溶解度变小 |
| C.风吹日晒使海水中的氯化钠蒸发 |
| D.风吹日晒使水分蒸发从而使氯化钠结晶析出 |
根据如图信息判断,下列叙述错误的是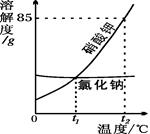
| A.硝酸钾的溶解度随温度升高而增大 |
| B.t1℃时,氯化钠和硝酸钾的溶解度相同 |
| C.要从含有少量氯化钠的硝酸钾溶液中得到较多的硝酸钾晶体,通常可采用降温结晶的方法 |
| D.t2℃时,80g硝酸钾溶于100g水中可制得饱和溶液 |
右图表示的是甲、乙两种固体物质的溶解度曲线,下列叙述一定正确的是
| A.甲的溶解度大于乙的溶解度 |
| B.10℃时甲、乙两溶液的质量分数相等 |
| C.30℃时甲的饱和溶液的质量分数为60% |
| D.降低温度可使接近饱和的甲溶液变成饱和溶液 |
向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤。下列说法正确的是( )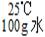
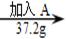 ①
① 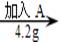 ②
② 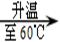 ③
③ 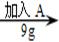 ④
④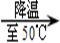 ⑤
⑤
资料:A的溶解度
| 温度/℃ | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 |
C.②中A的质量分数最大 D.①③④⑤为不饱和溶液
下表是NaCl、KNO3在不同温度时的溶解度: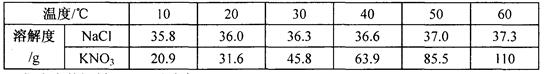
跟据表内数据判断,下列说法错误的是
| A.KNO3和NaCl的溶解度曲线在20℃~30℃相交 |
| B.60℃时,向105g KNO3的饱和溶液中加入95g水,所得溶液的溶质的质量分数为27.5% |
| C.从含有少量NaCl的KNO3饱和溶液中得到较多的KNO3晶体,通常采用冷却热饱和溶液的方法 |
| D.20℃时,NaCl和KNO3固体各35g分别加入两只各盛有100g水的烧杯中,充分搅拌后均能形成饱和溶液 |