KCl是一种常用的钾肥,其溶解度如下表。下列说法正确的是( )
| 温度/℃ | 0 | 20 | 40 | 60 |
| 溶解度/g | 27. 6 | 34.0 | 40.0 | 45.5 |
B.20℃时,100 g KCl饱和溶液中含KCI 34.0 g
C.40℃时,KCl饱和溶液的质量分数为40.0%
D.60℃的KCl饱和溶液降温至20℃,有晶体析出
右图是a、b、c三种物质的溶解度曲线。由图示判断下列说法中正确的是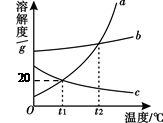
| A.a的溶解度随温度的升高而减少 |
| B.a的溶解度大于b的溶解度???? |
| C.c的饱和溶液从t2℃降温至t1℃时变为不饱和溶液? |
| D.t1℃时,60 g a的饱和溶液中含有溶剂50 g |
下列各项中,前者一定大于后者的是
| A.20℃时KNO3的溶解度、80℃时KNO3的溶解度 |
| B.30℃时NaCl不饱和溶液的质量分数、30℃时NaCl饱和溶液的质量分数 |
| C.碳酸镁中碳元素的质量分数、碳酸氢钠中碳元素的质量分数 |
| D.相同条件下:NaOH溶于水后溶液的温度、NH4NO3溶于水后溶液的温度 |
右图是甲、乙两种物质的溶解度曲线,下列叙述正确的是
| A.20℃时,甲的溶解度大于乙的溶解度 |
| B.40℃时,甲、乙两种物质的溶解度相等 |
| C.采用降温的方法可以将乙的不饱和溶液转化为饱和溶液 |
| D.60℃时,在100g水中加入100g甲,充分溶解后溶液质量为200g |
室温下,称取氯化钠和碳酸钠各30 g放同一烧杯中,加入100 g水充分搅拌后静置,得到二者的混合溶液。请参照氯化钠、碳酸钠两种物质的溶解度表判断,以下结论不正确的是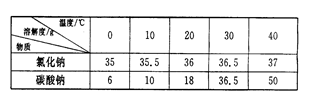
| A.20℃时,氯化钠的溶解度大于碳酸钠的溶解度 |
| B.20℃时,未溶解固体是氯化钠和碳酸钠的混合物 |
| C.30℃时,溶液中氯化钠和碳酸钠的质量分数相同 |
| D.30℃时,溶液为氯化钠和碳酸钠的不饱和溶液 |
右图是甲、乙两种固体物质的溶解度曲线。据此判断下列说法不正确的是: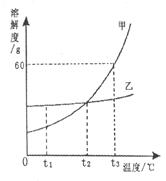
| A.t2℃时,甲、乙的溶解度相等 |
| B.t3℃时,将60g乙加入100g水中可得l60g溶液 |
| C.乙的溶解度受温度影响很小 |
| D.tl℃时,乙的溶解度大于甲的溶解度 |
下表给出了在20℃和100℃时X、Y两种化合物在不同溶剂中的溶解度数据,请分析有关数据,判断利用结晶法从X、Y的混合物中提纯X时,使用哪种溶剂的回收率最高(已知混合物含X70g,含Y15g)
| | 20℃时的溶解度/g | 100℃时的溶解度/g | ||
| 溶剂序号 | X | Y | X | Y |
| A | 20 | 5 | 90 | 30 |
| B | 15 | 1 | 70 | 10 |
| C | 5 | 15 | 75 | 25 |
| D | 10 | 12 | 80 | 20 |
下列事实中,能说明X物质的溶液在t℃时肯定是饱和溶液的有
①溶液中有大量的X物质 ②加入5gX时,有X固体未溶解
③加热蒸发掉一定水后再冷却到原温度时,会析出X晶体④冷却时有X晶体析出
| A.0个 | B.1个 | C.2个 | D.3个 |
现有50℃硝酸钾饱和溶液,欲使其成为不饱和溶液,可采用的方法有①降低温度②升高温度③增加溶质④减少溶剂⑤增加溶剂
| A.①③ | B.②④⑤ | C.①③④ | D.②⑤ |