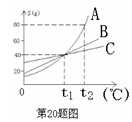
两种不含结晶水的固体物质甲、乙的溶解度曲线图如下图,下列说法正确的是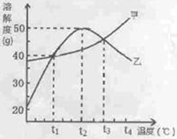
| A.t2℃时,乙的溶解度为50g |
| B.只有在t2℃时甲和乙的溶解度相等 |
| C.乙的溶解度随温度升高而增大 |
| D.分别把等质量的甲、乙两饱和溶液从t3℃降到t1℃时,两溶液析出晶体的质量相等 |
右图是固体物质R的溶解度曲线。将60 ℃ R的饱和溶液降温到20 ℃时,下列说法正确的是( )。
| A.溶液中溶质的质量分数不变 |
| B.溶液质量增加 |
| C.溶液中溶质的溶解度减小 |
| D.溶液变成不饱和溶液 |
(2011?杭州)下列变化中,溶液中原溶质的溶解度和溶质分量分数都发生变化的是( )
| A.常温下密闭容器中硝酸钾稀溶液升温100C |
| B.氯化铁溶液中加入少量生石灰 |
| C.硫酸锌溶液中加入少量铜粉 |
| D.稀释硫酸钠溶液 |
氯化铵和硫酸钠溶解度曲线如下图所示,从图中获取信息正确的是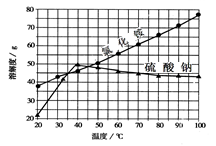
| A.20 ℃~40 ℃,氯化铵的溶解度大于硫酸钠 |
| B.两种物质溶解度都随温度升高而增大 |
| C.45 ℃时两种物质饱和溶液的溶质质量分数相等 |
| D.将50 ℃的硫酸钠饱和溶液降至20 ℃,始终没有晶体析出 |
右图是固体物质a、b、c的溶解度曲线图。根据此曲线图,下列的说法正确的是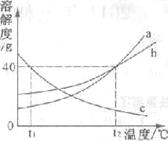
| A.t1℃时,a、b、c三种物质的溶解度大小顺序是a>b>c |
| B.t2℃时,a、b两种物质的饱和溶液的溶质质量分数相等 |
| C.t2℃时,将40g c物质加入到100g水中,形成的溶液是不饱和的 |
| D.t2℃时,欲使c物质的饱和溶液变为不饱和溶液,可以采用升高温度的方祛 |
甲、乙两固体物质的溶解度曲线如右图所示。下列说法不正确的是 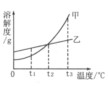
| A.t1℃时,甲物质的溶解度小于乙物质的溶解度 |
| B.t2℃时,甲、乙两物质的饱和溶液中分别含甲、乙两物质的质量相等 |
| C.将t3℃的甲、乙两物质的饱和溶液降温至t℃时,都会析出晶体 |
| D.甲、乙两物质的溶解度均随温度的升高而增大 |
以下是KCl的部分溶解度数据,下列说法中正确的是( )
| 温度/℃ | 0 | 20 | 40 | 60 |
| 溶解度/g | 27.6 | 34.0 | 40.0 | 45.5 |
B.20℃时,100g饱和KCl溶液中含KCl34.0g
C.20℃时,KCl溶液中溶质的质量分数一定小于40℃时溶液中溶质的质量分数
D.60℃时将溶质质量分数为30%的KCl溶液降温至40℃时,有晶体析出
甲、乙两种物质的溶解度曲线如图所示,下列叙述中,正确的是
| A.t1OC时,甲、乙各30g加入到70g水中,均能恰好完全溶解 |
| B.t1OC时,甲和乙的饱和溶液中溶质的质量分数相等 |
| C.t2OC时,在100g水中加入60g甲,所得溶液中溶质的质量分数为37.5% |
| D.t2OC时,分别在100g水中溶解20g甲、乙,同时降温,乙先达到饱和 |
20℃时,某物质溶解于水的实验数据如下表。则下列叙述正确的是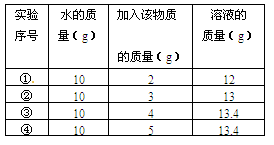
| A.②中所得溶液是饱和溶液 |
| B.20℃时10g水最多能溶解4g该物质 |
| C.③④溶液的溶质质量分数相等 |
| D.①所得溶液的溶质质量分数为20% |