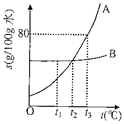
现有一杯20℃的饱和硝酸钾溶液,欲改变其溶质质量分数,下列方法可行的是
| A.升温到60℃ | B.恒温蒸发部分水 |
| C.加入一定量的水 | D.加入一定量的硝酸钾固体 |
根据右图判断,下列说法错误的是: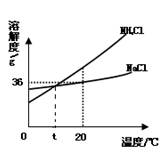
| A.NaCl和NH4Cl的溶解度都随温度升高而增大 |
| B.20℃时,18gNaCl加入到50g水中,搅拌后将全部溶解 |
| C.t℃时,NH4Cl饱和溶液和NaCl饱和溶液溶质质量分数相等 |
| D.将20℃时某NH4Cl溶液降温到0℃,其溶质质量分数一定减小 |
右图是甲、乙两种物质的溶解度曲线。在t2℃时向盛有100 g水的烧杯中先后加入w g甲 和w g乙(两种物质溶解时互不影响),充分搅拌。将混合物的温度降低到t1℃。下列说法正确的是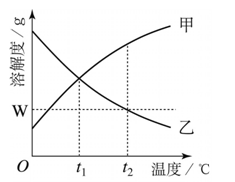
| A.甲物质的溶解度随温度升高而减小 |
| B.温度降低到t1℃时,得到甲、乙的饱和溶液 |
| C.温度降低到t1℃时,甲、乙的溶质质量分数相等,得到甲、乙的不饱和溶液 |
| D.t2℃时,甲物质的溶液为饱和溶液,乙物质的溶液为不饱和溶液 |
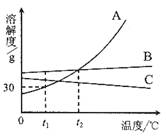
右图是a、b、c三种物质的溶解度曲线。由图示判断下列说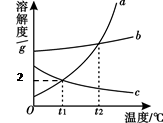 法中正确的是
法中正确的是
| A.a的溶解度随温度的升高而减少 |
| B.a的溶解度大于b的溶解度???? |
| C.c的饱和溶液从t2℃降温至t1℃时变为不饱和溶液? |
| D.t1℃时,60 g a的饱和溶液中含有溶剂50 g |
海水中溶有大量的盐,盐场利用海水晒盐获得粗盐,晒盐后得到的卤水中含有NaCl外还含有MgCl2、KCl和MgSO4等物质,右图是它们的溶解度曲线示意图。下列说法正确的是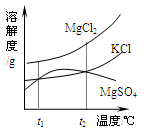
| A.温度的变化对MgCl2和KCl的溶解度影响不大 |
| B.将卤水加热到t2℃以上,析出的晶体主要是MgSO4 |
| C.盐场利用海水晒盐获得粗盐的过程中,主要发生化学变化 |
| D.t1℃时三种物质的溶解度的关系是:S(MgCl2)>S(KCl)>S(MgSO4) |
右图是甲、乙两种固体物质的溶解度曲线。下列说法正确的是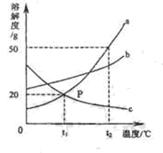
| A.a物质的溶解度为50g |
| B.t1℃时,a、c两物质的溶解度相等 |
| C.升高温度可使不饱和的a溶液变为饱和 |
| D.c物质的溶解度随温度的升高而增大 |
如图为氯化铵和硫酸钠的溶解度曲线。下列说法错误的是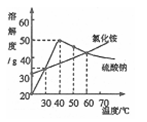
| A.氯化铵的溶解度随温度的升高而增大 |
| B.30℃时,氯化铵、硫酸钠的溶解度相同 |
| C.40℃时硫酸钠饱和溶液溶质的质量分数约为33.3% |
| D.将50℃时硫酸钠的饱和溶液降低温度,始终有晶体析出 |
下面是某学生对课本中图表资料的使用情况,其中不正确的是 ( )
| A.根据元素周期表可以判断元素在自然界的含量 |
| B.根据金属活动性顺序表,判断金属能否置换出稀硫酸中的氢 |
| C.根据溶解度曲线图,判断某物质在一定温度下的的溶解度 |
| D.根据酸、碱、盐的溶解性表,判断某些复分解反应能否进行 |