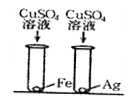
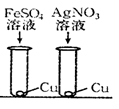
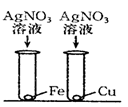
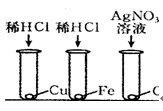
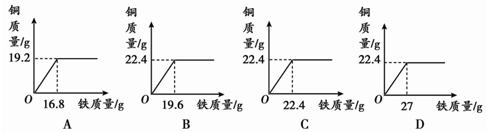
下列金属中,活动性最强的是
| A.铜 | B.铁 | C.镁 | D.银 |
向氯化铜和稀盐酸的混合溶液中,加入过量的铁粉,充分反应后过滤。下列关于上述过程的叙述正确的是
| A.滤液中一定含有FeCl3 | B.过滤后得到的固体可能是纯净物 |
| C.反应后固体的质量可能会增加 | D.反应后溶液的质量一定会减少 |
若金属锰(Mn)在金属活动性顺序中位于铝和锌之间,则下列反应不正确的是
| A.Mn + H2SO4 = MnSO4 + H2↑ | B.Mg + MnSO4 = MgSO4 + Mn |
| C.Fe + MnSO4 = FeSO4 + Mn | D.Mn + CuSO4 = MnSO4 + Cu |
现有甲、乙、丙三种金属,将甲、乙两种金属分别放入硫酸铜溶液中,甲表面有红色固体析出,乙没有明显现象;将甲、丙分别与相同的稀硫酸反应,甲比丙反应慢。下列金属活动性顺序的排列正确的是
| A.丙>甲>乙 | B.甲>乙>丙 |
| C.乙>甲>丙 | D.丙>乙>甲 |
铁和铜都能与氯化铁溶液反应,反应的化学方程式为:Fe + 2FeCl3 3FeCl2,Cu + 2FeCl3 CuCl2 + 2FeCl2 若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后烧杯中有金属剩余。下列分析正确的是
① 剩余金属只有Fe ② 剩余金属一定有Cu
③ 反应后的溶液中一定有FeCl2 ④ 反应后的溶液中可能有FeCl3
| A.①、③ | B.②、③ | C.②、④ | D.只有③ |
在CuO和Fe的混合物中加入一定量的稀硫酸,微热,待反应停止后过滤,滤出不溶物后再往滤液里加入一枚铁钉,若铁钉无变化,则正确的叙述是
| A.不溶物中可能有铜 | B.不溶物可能全部是铁 |
| C.滤液是硫酸亚铁溶液 | D.滤液是硫酸铜和硫酸亚铁的混合溶液 |
等质量的锌、铁、镁分别与足量的稀硫酸完全反应后生成氢气的质量 ( )
| A.锌最多 | B.铁最多 | C.镁最多 | D.无法判断 |