向氯化铜和氯化镁的混合溶液中加入一定量的锌粉充分反应,下列情况中可能出现的是( )
①溶液中有 Mg2+、Zn2+、Cu2+,不溶物为Cu ②溶液中有 Zn2+,不溶物为Mg、Cu
③溶液只有Mg 2+,不溶物为 Zn 、Cu ④ 溶液有Mg2+、 Zn2+,不溶物为 Zn 、Cu
| A.①③ | B.②③ | C.①④ | D.③④ |
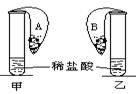
金属单质家族四兄弟W、X、Y、Z,不小心掉入稀盐酸池,神情如图所示:
则W、X、Y、Z的金属活动性顺序为( )
| A.X>W>Z>Y | B.Z>X>W>Y | C.W>X>Y>Z | D.Y>Z>X>W |
下列物质露置在空气中,质量都会发生改变,其中与空气中氧气和水都有关的是
| A.铁 | B.氢氧化钠 | C.氧化钙 | D.浓盐酸 |
某同学利用一黑色粉末(含氧化铜、碳粉、铁粉中的一种或多种)和未知溶质质量分数的稀硫酸,做如下探究:将a g黑色粉末加入到盛有50 g该稀硫酸的烧杯中,充分反应后称得烧杯内物质质量为(49.8+a)g。他对实验的推理正确的是
| A.反应后不可能得到红色固体 |
| B.黑色粉末中含有铁粉,加入黑色粉末质量一定为5.6 g |
| C.若反应后黑色粉末无剩余,则黑色粉末中一定不含有碳粉 |
| D.该稀硫酸中溶质的质量分数不低于19.6% |
现有甲、乙、丙、丁四种金属,将这四种金属粉末分别投人相同浓度的盐酸中,只有丙、丁发生反应并产生气泡,而且丁产生气泡比丙的更快;将甲投入乙的硝酸盐溶液中,有金属乙析出。这四种金属的活动性顺序是
| A.丁>丙>甲>乙 | B.乙>甲>丙>丁 |
| C.丙>丁>甲>乙 | D.丁>丙>乙>甲 |
现有甲、乙、丙三种金属,将甲、乙两种金属分别放入相同浓度的硫酸铜溶液中,甲表面有红色固体析出,乙没有明显现象;将甲、丙分别与相同浓度的稀硫酸反应,甲比丙反应速率快。根据以上实验事实,判断这三种金属的活动性由强到弱的顺序为
| A.丙、甲、乙 | B.甲、乙、丙 | C.乙、甲、丙 | D.甲、丙、乙 |
往硫酸和硫酸铜的混合稀溶液中,加入一定量的铁粉,若充分反应后,过滤得滤液和剩余固体,则依此推论正确的是( )
| A.滤液中一定有FeSO4 | B.剩余固体中一定没有Cu |
| C.滤液中一定有H2SO4 | D.剩余固体中一定有Fe |
往Cu(NO3)2、Zn(NO3)2的混合溶液中加入一些铁粉,待反应完成后再过滤,不可能的情况是
| A.滤纸上有Cu,滤液中有Cu2+、Zn2+、Fe2+ |
| B.滤纸上有Cu,滤液中有Zn2+、Fe2+ |
| C.滤纸上有Cu、Fe,滤液中有Cu2+、Zn2+、Fe2+ |
| D.滤纸上有Cu、Fe,滤液中有Zn2+、Fe2+ |
学习金属单元后,我们知道Zn、Fe、Cu三种金属的活动性顺序为:Zn>Fe>Cu。为验证这一结论,下面实验设计合理的是 ( )
| A.将Zn、Cu两金属片分别放入稀盐酸中 |
| B.将Fe、Cu两金属片分别放人稀盐酸中 |
| C.将Zn、Fe两金属片分别放人CuCl2溶液中 |
| D.将Zn、Cu两金属片分别放人FeCl2溶液中 |