碳酸钾 (K2CO3) 和硝酸钾 (KNO3) 在不同温度时的溶解度及其溶解度曲线如下:
| 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度 g/100g水 | K2CO3 | 110 | 114 | 121 | 126 | 139 |
| KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 |
 ① 30℃时K2CO3的溶解度为 (14) g/100g水。
① 30℃时K2CO3的溶解度为 (14) g/100g水。
② 图1中能表示KNO3溶解曲线的是 (15) (填“甲”
或“乙”)。
③ 曲线上M点的含义是 (16) 。
④ 要配制100g 10%的KNO3溶液,需要KNO3固体
(17) g。溶液配制过程中,除用到玻璃棒、胶头滴管外,
还需用到下 列仪器中的 (18) 。(填字母编号)
A.电子天平 B.烧杯 C.漏斗 D.量筒
⑤ 60℃时500g饱和KNO3溶液蒸发10g水后,再降温到60℃,可析出KNO3晶体 (19) g。
⑥ 40℃时,向两个分别盛有相同质量的硝酸钾和碳酸钾的烧杯中,各加入100g水,充分溶解后,恢复至40℃,其结果如图2所示。下列有关说法中,正确的有 (20) 。(填字母编号)
 A.烧杯①中溶解的是KNO3,烧杯②中溶解的是K2CO3
A.烧杯①中溶解的是KNO3,烧杯②中溶解的是K2CO3
B.烧杯②中溶液是不饱和溶液
C.升高温度或增加溶剂都有可能将烧杯①中固体全部溶解
D.若将烧杯①中的溶液变为不饱和溶液,溶液中溶质质量分数
一定减小
二氧化碳的“捕捉”与“封存”是实现温室气体减排的重要途径之一。实际生产中,经常利用足量NaOH溶液来“捕捉”CO2,流程图如下(部分条件及物质未标出)。
 |
① 分离室中进行的操作是 (9) 。
② 该流程图所标出的物质中,溶于水放出大量热的氧化物是 (10) ,与 水发生反应的化学方程式为 (11) 。
水发生反应的化学方程式为 (11) 。
③ “捕捉室”中发生的化学反应为2NaOH CO2 → Na2CO3
CO2 → Na2CO3 M,则M的化学式为 (12) ;整个“捕捉”过程中,可循环使用的物质是 (13) 。
M,则M的化学式为 (12) ;整个“捕捉”过程中,可循环使用的物质是 (13) 。
多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界。
① 根据下表提供的信息,填写有关含碳物质的对应特征。
| 物质用途 | 石墨作电极 | 活性炭净水 |
| 对应特征 | 导电性 | (1) |
② 某矿石中含碳、硅、氧、铁、钙等多种元素,其中地壳中含量最多的元素是 (2) 。
③ 碳元素形成的单质有金刚石、石墨、C60,这些物质互称为碳元素的 (3) 。
④ CO2常用于灭火,但镁着火不能用 CO2灭火,原因是它们发生反应生成氧化镁和碳,该反应的化学方程式 (4) ;其中发生氧化反应的物质是 (5) 。
⑤ 高温下,A、B两种物质可以发生化学反应生成C和D。反应前后分子种类变化的微观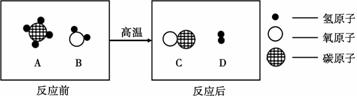 示意图如下所示。
示意图如下所示。
A代表的是 (6) (填化学式);四种物质中,可用作燃料的是 (7) (填上图中的字母);在该反应中,生成C和D的物质的量之比为 (8) 。
。
密闭容器内,将少量乙醇(化学式C2H5OH)置于一定 量氧
量氧 气中燃烧,生成二氧化碳、水蒸汽和一种未知物质W。现测得反应前后各物质的质量如下:
气中燃烧,生成二氧化碳、水蒸汽和一种未知物质W。现测得反应前后各物质的质量如下:
| 物质 | 乙醇 | 氧气 | 二氧化碳 | 水 | W |
| 反应前质量/g | 48 | 80 | 0 | 0 | 0 |
| 反应后质量/g | 2 | 0 | 44 | 54 | X |
下列说法错误的是
A.W物质一定含有氧元素 B.该反应属于氧化反应
C.W物质一定含有氢元素 D.表中X的值为28
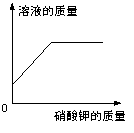
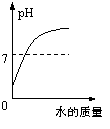
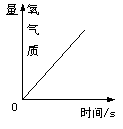
下列四个图像 中,能正确表示对应变化关系的是
中,能正确表示对应变化关系的是
 | |||||
 |  |
|
|
|
| ||||||||
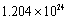 个铜原子
个铜原子 燃着的木条鉴别氧气与二氧化碳
燃着的木条鉴别氧气与二氧化碳 氧化钙
氧化钙