小明发现一种淡黄色的粉末可以用于杀菌、消毒和漂白,于是想探究该固体的成分。
[提出问题] 该淡黄色固体的化学成分是什么?
[查阅资料]
(1)硫单质是一种淡黄色固体,难溶于水,在空气中点燃硫单质,生成一种无色、有刺激性气味的气体。
(2)过氧化钠(Na2O2)是一种淡黄色固体,能与水反应,生成气体并放出大量的热。
[设计实验方案]
方案一:取少量该固体粉末于试管中,加2mL水,振荡并观察现象。
方案二:在燃烧匙里放少量该固体,在酒精灯上加热,观察现象。
比较以上两方案,你认为的最佳方案是 ,理由 是(从环保、操作等角度分析)
是(从环保、操作等角度分析)
。
[实验验证并得出结论]
小明向盛有少量该固体的试管中加入2mL水,立刻观察到有无色气泡产生,并且验证出该反应同时生成了氢氧化钠(NaOH)。通过实验验证,确定该淡黄色粉末为过氧化钠。
小明想对生成的气体成分判断,他提出了以下两种假设:
①该气体是CO ②该气体是O2
你认为上述假设哪个更合理?并说明选择的理由。
。
请设计一个实验,验证你的合理假设(写出简要操作步骤、实验现象和结论)。
| 操作步骤 | 实验现象 | 结论 |
[计算] 在过氧化钠(Na2O2)中,①氧元素的化合价为 ;
②过氧化钠中钠、氧元素的质量比为 ;
① 78克过氧化钠与多少克二氧化碳中所含氧元素的质量相等?(列式计算 )
(1) 化学用语是学习化学的重要工具,请用化学用语填写下列空格。
2个氮分子 ; 五氧化二磷中磷元素显+5价 ;
保持水的化学性质的最小粒子是 ;
“过氧化氢分解”变化中最小的粒子是 。
(2)元素周期表是学习和研究化学的重要工具。请根据下表(元素周期表的部分内容)回答有关问题:
|
 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | ||
| 2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 | ||
| 3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
①请 从上表中查出关于硼元素的一条信息:_______________
从上表中查出关于硼元素的一条信息:_______________ ____________。
____________。
②16号元素的原子在化学变化中比较容易 (选填“得”或“失” )电子,形成的粒子符号为 。
③第11号元素与第17号元素组成的化合物化学式是 ,构成该物质的
粒子是 (选填“分子”、“原子”或“离子”)。
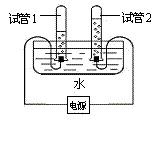 (5)小刚利用右图所示装置探究水的组成。
(5)小刚利用右图所示装置探究水的组成。 化情况。实验完毕,甲同学的广口瓶内水面上升明显大于瓶内空气体
化情况。实验完毕,甲同学的广口瓶内水面上升明显大于瓶内空气体 这两种现象解释合理的是
这两种现象解释合理的是 