下列对一些事实的解释错误的是( )。
| 事实 | 解释 | |
| A | 书写档案规定必须使用碳素墨水 | 碳的化学性质稳定 |
| B | 石墨能够做电池的电极材料 | 石墨能够导电 |
| C | 焦炭可以把铁从它的氧化物矿石里还原出来 | 焦炭具有氧化性 |
| D | 制糖工业中用活性炭来脱色以制白糖 | 活性炭具有吸附性 |
为进一步研究高锰酸钾的分解产物,某兴趣小组同学查阅资料,并取一定质量的高锰酸钾加热使之完全分解,然后分别进行了以下三个实验。
| 编号 | 实验内容 | 实验现象 | 实验结论 |
| 1 | 取反应后固体剩余物0.2g加入5mL 6%的H2O2溶液中 | 剧烈反应,放出大量热量,产生大量气体 | 固体剩余物中的MnO2对H2O2分解有催化作用 |
| 2 | 取0.2gMnO2加入5mL a▲ (H2O2溶液的质量分数)的H2O2溶液中 | 平稳反应,放出热量,持续产生气体 | MnO2对H2O2分解有催化作用 |
| 3 | 取反应后固体剩余物1.0g加入足量水中,充分溶解,过滤 | 固体完全溶解,滤纸上无黑色固体残余物 | 固体剩余物中无 b ▲ |
【实验内容】:
【实验分析】
(1)完成上表中的填空内容:a ▲ 、b ▲ ;
(2)实验2的目的是 ▲ ;
(3)同学们经过讨论,认为实验1的结论不正确,理由是 ▲ ;
【查阅资料】
Ⅰ、KMnO4受热分解时,在某条件下可能发生以下两个反应:
① 6KMnO4  2K2MnO4 + K2Mn4O8 + 4O2↑
2K2MnO4 + K2Mn4O8 + 4O2↑
② KMnO4  KMnO2 + O2↑
KMnO2 + O2↑
Ⅱ、相对分子质量:(KMnO4:158 O2:32)
(4)16gKMnO4中氧元素的质量为 ▲ ;加热使之完全分解,若完全发生反应①,生成O2的质量为 ▲ ;若同时发生反应①②,生成O2的质量范围是 ▲ 。(保留二位小数。提示:依据质量守恒定律观察)
实验室有下列装置,请根据要求回答问题:
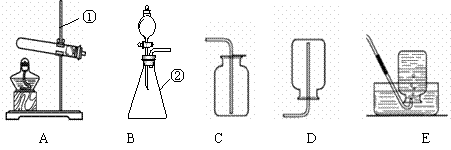 |
(1)写出有标号仪器的名称:① ▲ ;② ▲ ;
(2)检查B装置的气密性的方法是:堵住右侧导气管, ▲ ,向分液漏斗中加适量的水,若观察到分液漏斗末端出现稳定的水柱,则装置不漏气;
(3)实验室用过氧化氢溶液和二氧化猛制取氧气的化学方程式为 ▲ , 选用的发生装置为 ▲ (填序号);
(4)实验室用高锰酸钾制取氧气并用于验证蜡烛燃烧产物的实验,选用的收集装置为 ▲ (填序号);如何判断该装置已收集满氧气 ▲ ;
(5)实验室用高锰酸钾制取氧气并用排水法收集,主要实验步骤有:⑴装药品;⑵检查装置气密性;⑶加热;⑷装置固定在铁架台上;⑸熄灭酒精灯;⑹收集气体;⑺将导管移出水槽。正确的操作顺序为 ▲
A、⑴⑵⑶⑷⑸⑹⑺ B、⑵⑴⑷⑶⑹⑸⑺
C、⑴⑵⑷⑶⑹⑸⑺ D、⑵⑴⑷⑶⑹⑺⑸
定量研究对于化学科学发展有重大作用,因此我们应该掌握好有关质量守恒定律的相关知识。
(1)下图A、B、C三个实验用于验证质量守恒定律,其中不能达到实验目的的是 ▲
(选填序号),理由是 ▲ 。
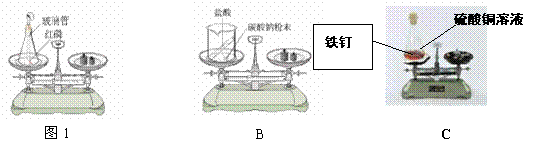 |

(2)自然界中绿色植物光合作用可用下式表示:CO2 + H2O 淀粉 + O2
① 分析化学反应前后元素种类可知:淀粉中一定含有的元素是_ ▲___(填元素符号),可能含有的元素是__▲__(填名称)。
② 在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
| 物质 | A | B | C | D |
| 反应前质量/g | 2 | 24.5 | 4 | 8 |
| 反应后质量/g | 16.9 | 0 | 13.6 | X |
表中X=___▲___,在反应中D这种物质可能起__ _▲_ _ 作用。容器内发生反应的基本类型是___▲___(选填:化合反应或分解反应)。