硝酸铵是农村常用的化肥。右图为某硝酸铵化肥外包装袋说明。
(1)通过计算说明该硝酸铵化肥是混合物。
(2)计算该化肥中硝酸铵的质量。
| 硝酸铵 (NH4NO3) 净重:50kg 含氮量:34.3% ΧΧ化学工业公司 |
为验证质量守恒定律,某学习小组使用如图所示的装置进行实验:
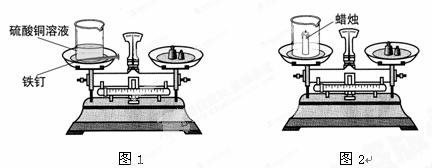 |
实验一:如图1,将盛有硫酸铜溶液的烧杯和用砂纸打磨干净的铁钉一起放在托盘天平上称量,天平平衡后,将铁钉浸到硫酸铜溶液中,一段时间后,观察现象。
实验二:如图2,同学们又用此装置做蜡烛在氧气中燃烧实验。
(1)实验一中,学生观察到溶液由蓝色逐渐变成绿色,铁钉表面有红色物质析出,说明 ,实验中还应观察到的现象是 。
(2)实验二中,学生没有得出正确的实验结论,分析原因并改进实验方案。
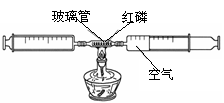 在测定空气中氧气含量的实验中,小强采
在测定空气中氧气含量的实验中,小强采
用了右图所示装置:在由两个注射器组成的密闭
系统中留有25mL空气,给装有红磷的玻璃管加热,同时
缓慢推动两个注射器活塞,充分反应后停止加热,
待冷却至室温,将气体全部推至一个注射器内,
观察密闭系统内空气体积变化。
(1)红磷燃烧的现象 ,反应的化学方程式为 。
(2)在实验加热过程中,交替缓慢推动两个注射器活塞的目的是 。
 (3)小强测得实验结果如下:
(3)小强测得实验结果如下:
| 反应前注射器内气体总体积 | 反应后注射器内气体总体积 |
| 25mL | 22mL |
由此数据可以推算出他测定的空气中氧气的体积分数 2l%。造成该实验出现误差的可能原因之一是 。
 D.打扫教室时,先喷洒水后扫地
D.打扫教室时,先喷洒水后扫地
 学性
学性 到的玻璃仪器是( )
到的玻璃仪器是( ) 烧杯、玻璃棒 B、量筒、烧杯、集气瓶
烧杯、玻璃棒 B、量筒、烧杯、集气瓶 的一些装置,据图回答有关问题。(填装置序号)
的一些装置,据图回答有关问题。(填装置序号)