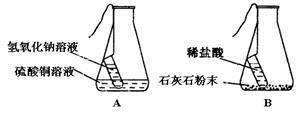
小强同学前往当地的石灰石矿区进行调查,他 取回了若干块矿石样品,对样品中碳酸钙的质量分数进行检测,采用的办法如下:取用8 g这种石灰石样品,把40 g稀盐酸分4次加入,测量过程所得数据见下表(已知石灰石样品中含的杂质不溶于水,不与盐酸反应)。请计算:
取回了若干块矿石样品,对样品中碳酸钙的质量分数进行检测,采用的办法如下:取用8 g这种石灰石样品,把40 g稀盐酸分4次加入,测量过程所得数据见下表(已知石灰石样品中含的杂质不溶于水,不与盐酸反应)。请计算:
| 序号 | 加入稀盐酸质量/g | 剩余固体质量/g |
| 第1次 | 10 | 5.5 |
| 第2次 | 10 | m |
| 第3次 | 10 | 1.2 |
| 第4次 | 10 | 1.2 |
(1)8 g石灰石样品中含有杂质多少克?
(2)样品中碳酸钙的质量分数是多少?
(3)上表中m的数值应该为多少?
(4)要得到280 kg CaO,需要质量分数为80%的石灰石多少千克?(化学方程式:CaCO3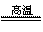 CaO+CO2↑)
CaO+CO2↑)
配平下列化学方程式:
|
|
(3)Al+ O2 —— Al2O3
|
(5)Cu2(OH)2CO3 —— CuO +H2O +CO2↑
下表是混有甲烷的空气在有限空间内点燃时的现象:
| 混合气中甲烷的体积分数 | 2.0% | 4.0% | 5.0% | 6.0% | 9.0% | 10.0% | 15.0% | 16.0% | 18.0% |
| 点燃时的现象 | 不爆炸 | 不爆炸 | 爆炸 | 爆炸 | 强烈 爆炸 | 爆炸 | 爆炸 | 燃烧 | 燃烧 |
(1)写出甲烷爆炸的化学方 程式___________________________。
程式___________________________。
(2)若在有限的空间内甲烷与空气按1∶6的体积比混合,点燃时的现象为___________。
(3)煤矿的矿井里常含有甲烷,你认为煤矿应采取的安全措施是______________________。

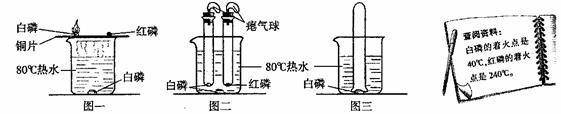 【知识回忆】可燃物燃烧的必备条件是 ;
【知识回忆】可燃物燃烧的必备条件是 ; 磷(如图三所示),结果观察到了“水火相容”的奇观,则大试管所装气体可能是 ;
磷(如图三所示),结果观察到了“水火相容”的奇观,则大试管所装气体可能是 ;