在学习碳酸钠的性质的课堂上,老师在碳酸钠溶液中加入一定量的澄清石灰水产生白色沉淀, 在滤出沉淀后,老师引导同学们对滤液中溶质的成分进行探究。同学们通过讨论认为溶质是NaOH、Na2CO3、Ca(OH)2中的一种或两种,其可能情况有三种:①NaOH;②NaOH和Na2CO3;③ 。
小伟同学设计了下列实验方案,请你帮助完成。
| 实 验 步 骤 | 可能出现的实验现象 | 实验结论 |
| ⑴取少量滤液于试管中,加入碳酸钠溶液 | 产生 | 假设③成立 |
| ⑵取少量滤液于试管中,加入足量稀盐酸 | 放出无色气体 | 假设 成立 |
| ⑶取少量滤液于试管中,加入碳酸钠溶液或足量稀盐酸 | 没有明显现象 | 假设 成立 |
小强根据小伟设计的实验方案,在滤液中加入足量稀盐酸,观察到有大量气泡产生,产生该现象化学方程式为 。因此他得出的结论是只有假设 成立,若该假设成立说明教师做的实验
是 (选填“恰好完全反应”、“Ca(OH)2过量”或“Na2CO3过量”)
某同学为了探究金属锰的一些性质,做了如下探究:
(1)将金属锰投入稀盐酸中,锰表面有气泡冒出。则金属锰在金属活动性顺序表中排在氢的 (选填“前面”或“后面”)。
(2)为了比较锰与铁的活动性大小,该同学设计下列方案进行实验,请完成下表:
| 猜想 | 验证方法 | 现象 | 结论 |
| 锰的活动性比铁 填“大”或“小” | 将锰投入 溶液中 | 锰表面有黑色的物质析出 | 猜想正确 |
(3)请根据上述的信息,标出金属Fe、Mn、Cu在下列金属活动性顺序表中的相应位置。

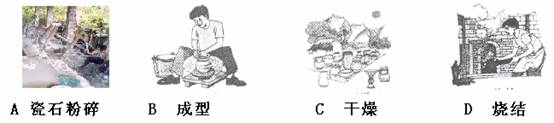
 完全反应后,称得烧杯内剩余物质的总质量
完全反应后,称得烧杯内剩余物质的总质量
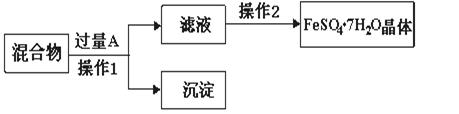
 用硫酸亚铁废液(含少量硫酸铜和稀硫酸),制备硫酸亚铁晶体并进行如下实验。制备硫酸亚铁晶体主要的操作流程如下:
用硫酸亚铁废液(含少量硫酸铜和稀硫酸),制备硫酸亚铁晶体并进行如下实验。制备硫酸亚铁晶体主要的操作流程如下: