小超同学在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度。于是他对所得溶液的酸碱性进行探究 。
。
【探究目的】探究所得溶液的酸碱性
【提出猜想】所得溶液可能呈中性,也可能呈 性,还可能呈 性。
【实验验证】
| 实验操作 | 实验现象 | 结论 |
| 用试管取该溶液1-2mL,滴入1-2滴无色酚酞试液,振荡 | 无色酚酞试液变 | 溶液呈碱性 |
| 无色酚酞试液不变色 | 溶液呈 |
【分析与思考】
(1)若溶液呈碱性,则溶液中使其呈碱性的离子是  (填写微粒符号),为避免碱性溶液污染环境,小杨对所得溶液进行了如下处理:向溶液中逐滴加入M
(填写微粒符号),为避免碱性溶液污染环境,小杨对所得溶液进行了如下处理:向溶液中逐滴加入M gCl2溶液,直到不再产生沉淀为止
gCl2溶液,直到不再产生沉淀为止 。然
。然 后过滤,把滤液倒入蒸发皿中加热,得到氯化钠晶体,该过程涉及的化学方程式为 。
后过滤,把滤液倒入蒸发皿中加热,得到氯化钠晶体,该过程涉及的化学方程式为 。
(2)若无色 酚酞试液不变色,为了进一步确定溶液的酸碱性,请你设计新的方案来验证:(答对两个方案奖励2分,但化学试卷总分不超过60分。)
酚酞试液不变色,为了进一步确定溶液的酸碱性,请你设计新的方案来验证:(答对两个方案奖励2分,但化学试卷总分不超过60分。)
方案一: ______________
______。
方案二: _____________________
______。
通过化学学习,你已经掌握了实验室制取气体的一般规律,以下是老师提供的一些实验装置。
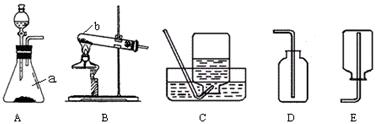 |
请结合上图仪器回答问题:
(1)写出图中标号的仪器名称:a ,b 。
(2)写出实验室用B装置制取氧气的化学方程式 。
 (3)通过查阅资料得知:①氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水,显碱性;②氨气在加热条件下能与
(3)通过查阅资料得知:①氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水,显碱性;②氨气在加热条件下能与 氧化铜反应生成铜、水和空气中含量最多的气体。小洁同学加热氯化铵和氢氧化钙的固体混合物制取氨气,她应选择的反应发生装置是(填字母编号,下同) ,收集装置是 。
氧化铜反应生成铜、水和空气中含量最多的气体。小洁同学加热氯化铵和氢氧化钙的固体混合物制取氨气,她应选择的反应发生装置是(填字母编号,下同) ,收集装置是 。
(4)小白将收集满氨气的集气瓶倒扣在滴有无色酚酞的水中,观察到的现象是
、 。
(5)请写出氨气和氧化铜在加热条件下反应的化学方程式 。
某同学模仿物理课上学到的“串联电路”,设计了如下气体制取与性质验证的组合实验。打开分液漏斗活塞后,A中出现大量气泡,B中白磷燃烧,C中液面下降,稀盐酸逐渐进入D中。请看图回答问题:
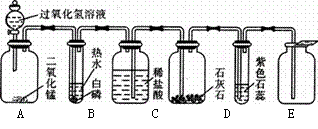 |
(1)A中发生反应的化学方程式为 。
(2)B中白磷能够燃烧的原因是 。
(3)E中的实验现象是  ,写出其中反应的化学方程式 。
,写出其中反应的化学方程式 。
(4)用F装置收集气体的依据是 。

 .元素钚-239的中子数为145 D.钚-239不会因为其放射性而具有一定的危险性
.元素钚-239的中子数为145 D.钚-239不会因为其放射性而具有一定的危险性