在宏观、微观和符号之间建立联系是化学学科的特点。
(1)在水、铜、氯化钠三种物质中,由分子构成的物质是 ,由离子构成的物质是 ,由原子构成的物质是 。
(2)“用微粒的眼光看世界”是我们学习化学的重要思想方法。试根据以下材料,结合你所学过的知识,回答下列问题:
材料1:一滴水(约为0.05克)里大约有15万亿亿个水分子,如果10亿人来数,每人每分钟数100个,日夜不停,约需3万多年。
材料2:洋葱被誉为“蔬菜皇后”。切洋葱时可闻到刺激性气味。
材料1说明 。
材料2说明 。
(3)A、B、C、D表示4种物质构成粒子的微观示意图,见下表:
| 物质 | A | B | C | D |
|
| 微观示意图 |
|
|
|
|
请回答以下问题:
①1个A分子中含有_____个原子。
② B中硫元素的化合价为 ;B中硫元素与氢元素的质量比 。
③4种物质中,属于化合物的是_____(填图中字母)。
④A和B反应生成C和D,写出此反应的化学方程式 。
在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
| 物质 | A | B | C | D |
| 反应前质量/g | 4 | 6 | 111 | 4 |
| 反应后质量/g | 待测 | 15 | 0 | 84 |
下列说法正确的是
A.该反应的反应物为A和C
B.容器中发生的化学反应,属于化合反应
C.反应后,生成D的质量为84g
D.反应后,待测A的质量为26g
 少量该固体的试管中加入2mL水,立刻观察到有无色气泡产生;再向试管中滴加几滴酚酞试液,可观察到溶液变红。小明判断反应生成了氢氧化钠(NaOH)和一种无色气体,并对生成的气体成分提出了以下三种假设:
少量该固体的试管中加入2mL水,立刻观察到有无色气泡产生;再向试管中滴加几滴酚酞试液,可观察到溶液变红。小明判断反应生成了氢氧化钠(NaOH)和一种无色气体,并对生成的气体成分提出了以下三种假设: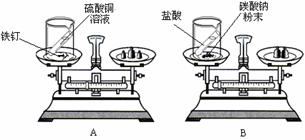
 发生反应的化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2
发生反应的化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2 ①造成天平的指针向右偏转的原因是 。
①造成天平的指针向右偏转的原因是 。
 A、B、C、D是我们学过的四种常见物质,其中三种为氧化物,一种为单质,D是一种黑色的固体。它们之间存在着如图所示的关系。(“ ”表示转化关系)
A、B、C、D是我们学过的四种常见物质,其中三种为氧化物,一种为单质,D是一种黑色的固体。它们之间存在着如图所示的关系。(“ ”表示转化关系)





 是 (填序号)。实验②中试管1所收集的气体为 (填化学式),此实验说明水是由 组成的。实验③中小卵石和石英砂的作用是 ,活性炭的作用是 。
是 (填序号)。实验②中试管1所收集的气体为 (填化学式),此实验说明水是由 组成的。实验③中小卵石和石英砂的作用是 ,活性炭的作用是 。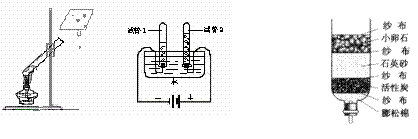
 Mn元素的质量分数)。下列选项中正确的是
Mn元素的质量分数)。下列选项中正确的是