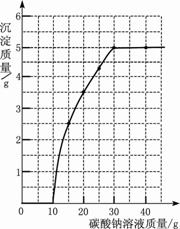
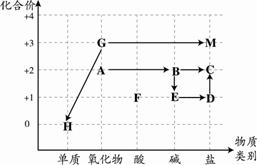
研究盐类物质的性质时,甲、乙、丙三位同学分别向NaHCO3溶液中滴加石灰水,均产生白色沉淀。他们分别设计实验方案,对自己过滤后的滤液中溶质的成分进行如下探究。
【实验准备】
用一定溶质的质量分数的NaHCO3溶液、NaOH溶液和Na2CO3溶液进行如下实验,为设计实验方案提供参考。
| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入酚酞溶液 | 溶液变红 | 现象Ⅰ | 溶液变红 |
| 加入CuSO4溶液 | 产生气泡和蓝色沉淀 | 现象Ⅱ | 产生气泡和蓝色沉淀 |
| 加入CaCl2溶液 | 无明显变化 | 无明显变化 | 产生白色沉淀 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
表中的现象Ⅰ为 ;现象Ⅱ为产生蓝色沉淀,对应反应的化学方程式是 。
【查阅资料】
(1)氯化钙溶液显中性。(2)滤液中所含的溶质有以下几种可能:
①NaOH;②Na2CO3;③NaOH和Ca(OH)2;④Na2CO3和NaHCO3;⑤Na2CO3和NaOH
【实验及分析】
甲同学:取少量滤液于试管中,滴加过量的稀盐酸,产生大量无色气泡,则滤液中的溶质是Na2CO3。
乙同学:取少量滤液于试管中,向其中通入少量CO2,产生白色沉淀,则滤液中的溶质是NaOH和Ca (OH)2。
(OH)2。
丙同学:分别取少量滤液于两支试管中,向一支试管中滴加CaCl2溶液,有白色沉淀产生;将另一支试管中的滤液 加热至沸腾,将产生的气体通入澄清石灰水,澄清石灰水变浑浊,则滤液中的溶质是Na2CO3和NaHCO3。
加热至沸腾,将产生的气体通入澄清石灰水,澄清石灰水变浑浊,则滤液中的溶质是Na2CO3和NaHCO3。
【反思与评价】
(1)老师认为乙、丙同学的实验方案和结论合理。
① 丙同学的实验中,加入CaCl2溶液的目的是 。
② 根据乙同学的结论,NaHCO3溶液与澄清石灰水反应的化学方程式是 。
(2)老师认为甲同学的实验方案和结论存在不足。丁同学通过以下实验帮助甲同学确认了滤液中溶质的成分。
| 实验操作 | 实验现象 | 实验结论 |
| _______________________________ _______________________________ | __________________________ __________________________ | 滤液中的溶质是Na2CO3和NaOH |
(3)结合此次探究活动,你认为下列说法正确的是__________(填字母序号)。
a.盐溶液可能显碱性
b.化学反应的产物与反应物的量有关http://ww w.xkb1.com
c.碱和盐反应一定生成另外一种碱和另外一种盐
d.判断溶液混合后的成分不仅要考虑产物,还要考虑反应物是否过量
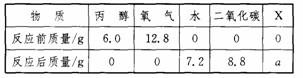 A.表中a的值为2.8
A.表中a的值为2.8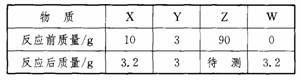 A.E可能是单质
A.E可能是单质