下列物质中,属于合成材料的是( )
|
| A. | 棉花 | B. | 羊毛 | C. | 塑料 | D. | 天然橡胶 |
人体中生命必需元素含量的多少直接影响人的健康,缺少某种元素可能导致骨质疏松,该元素是( )
|
| A. | 碘 | B. | 铁 | C. | 锌 | D. | 钙 |
空气中含量较多且性质活泼的气体是( )
|
| A. | 氧气 | B. | 氮气 | C. | 二氧化碳 | D. | 水蒸气 |
放学了,妈妈为小刚准备了如下的食谱.主食:馒头;配菜:红烧肉、豆腐汤.你认为食谱中还应添加( )
|
| A. | 醋溜白菜 | B. | 清蒸鱼 | C. | 炒鸡蛋 | D. | 牛奶 |
生活中的下列变化,属于化学变化的是( )
|
| A. | 冰块融化 | B. | 瓷碗破裂 | C. | 食物腐烂 | D. | 酒精挥发 |
为探究“酸碱中和反应”,进行了如下研究。
【实验原理】将稀HCl滴入盛有NaOH溶液的烧杯中,反应的化学方程式为 ;
【提出问题】实验中未观察到明显现象,同学们对该反应是否发生提出了疑问:反应后溶液中溶质是什么?
【假设猜想】溶液中的溶质有氯化钠,还可能有:
猜想1:HCl
猜想2:NaOH
猜想3:HCl和NaOH
你认为上述猜想不合理的是 。
【实验方案】(1)某同学用一支洁净试管取少量烧杯中的溶液,滴加FeCl3溶液,无明显现象,说明烧杯中溶液里一定不含 ;
(2)为了验证其余猜想,各小组进行如下三个方案的探究。
| 实验方案 | 甲 | 乙 | 丙 |
| 实验操作 |
|
|
|
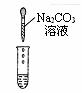
| 实验现象 | 试纸变色,对比比色卡,pH<7 |
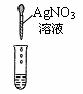
| 产生白色沉淀 |
| 实验结论 | 溶液中有HCl | 溶液中有HCl | 溶液中有HCl |
【推论与分析】上述实验方案中有两处明显错误:
 ①实验操作中的错误是 ;
①实验操作中的错误是 ;
②实验结论中有一个是错误的,错误的原因是 ;
通过对上述实验的正确操作,同学们得出了正确的结论。
你认为【假设猜想】中 是正确的。
(3)在20g10%的氢氧化钠溶液中加入25g稀盐酸恰好完全反应。
计算25g稀盐酸中溶质的质量分数 (计算结果精确到0.1%)。

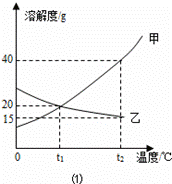
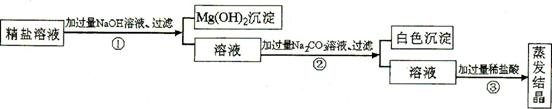
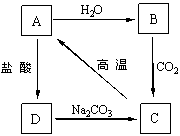 相互转化关系,回答下列问题:
相互转化关系,回答下列问题: