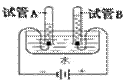
某活动小组的同学在探究金属与酸反应时,发现铜与浓硫酸在加热条件下能够发生反应,并产生大量气体。
【提出问题】产生气体的成分是什么呢?
【分析讨论】经分析讨论,大家认为产生的气体可能是H2、SO2、SO3、O2等气体,经进一步查验后确认没有SO3、O2,于是大家决定进一步探究气体成分。
【提出猜想】
猜想①:产生的气体仅为SO2;
你认为猜想②: ;
猜想③:产生的气体为SO2和H2的混合气。
【查阅资料】1、H2能燃烧,不能使红色品红溶液褪色。
2、SO2不能燃烧,能使红色的品红溶液褪色,是一种有毒气体,
化学性质与CO2相似。
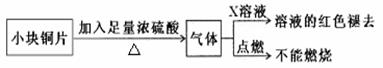
【设计实验】该小组的同学据此设计并完成了如图所示的实验:
 |
【分析与结论】
(1)图中X为 溶液。
(2)由以上实验可知:猜想 ( 填①或②或③)正确。
填①或②或③)正确。
【反思与评价】
(3)实验结束后,有同学认为多余的气体应通入一个装有NaOH溶液的烧杯中,
其原因是 。
 右图是关于盐酸化学性质的知识网络,
右图是关于盐酸化学性质的知识网络,

 “—”表示相连的两种物质能发生反应
“—”表示相连的两种物质能发生反应 ,
,

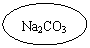
|

 质,A是含三种元素的化合物,与图中其
质,A是含三种元素的化合物,与图中其
|
 (1)写出A的化学式 。
(1)写出A的化学式 。
(2)反应①的化学方程式是 。
(3)根据该知识网络写出一个复分解反应化学方程式 。
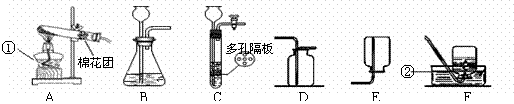 根据下列装置图,回答有关问题:
根据下列装置图,回答有关问题: 要使B物质的饱和溶液变成不饱和溶液,可以采取的一种方法是
要使B物质的饱和溶液变成不饱和溶液,可以采取的一种方法是 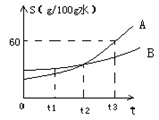
 碳家族是化学世界中最庞大的家族,碳及其化合物在生产生活中有着广泛
碳家族是化学世界中最庞大的家族,碳及其化合物在生产生活中有着广泛 (1)下列制品中,主要利用金属导电性的是 (填序号)。
(1)下列制品中,主要利用金属导电性的是 (填序号)。 (1)右图是电解水实验的示意图,试管A中产生的气体
(1)右图是电解水实验的示意图,试管A中产生的气体