下列体育用品中,不含有机合成材料的是( )
|
| A. | 铅球 | B. | 乒乓球 | C. | 排球 | D. | 运动鞋 |
下列实验操作中,正确的是( )
|
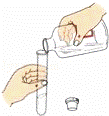
| A. |
倾倒液体 | B. |
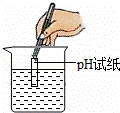
测溶液pH | C. |
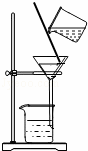
过滤 | D. |
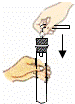
塞紧橡胶塞 |
下列物质中属于氧化物的是( )
|
| A. | O2 | B. | P2O3 | C. | KClO3 | D. | NaHCO3 |
下列属于物理变化的是( )
|
| A. | 食物腐败 | B. | 大米酿酒 | C. | 蜡烛熔化 | D. | 钢铁锈蚀 |
空气中体积分数最大的气体是( )
|
| A. | 氧气 | B. | 氮气 | C. | 二氧化碳 | D. | 稀有气体 |
化学兴趣小组的同学用实验室久置的氢氧化钠固体配置成溶液后,做酸碱中和反应实验,将稀盐酸滴入溶液中,观察到有气泡产生,同学们推测可能是氢氧化钠固体久置发生了变质。
【分 析】 氢氧化钠变质的原因是(用化学方程式表示) 。
【提出问题】该氢氧化钠固体是全部变质还是部分变质?
【查阅资料】氯化钙溶液和氯化钠溶液均呈中性
【设计实验】依据查阅的资料设计实验如下表所示
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量固体于试管中,加水配置成溶液,往其中滴加过量氯化钙溶液,并不断振荡。 | 有________ 生成 | 说明原固体中一定含有碳酸钠。 反应的化学方程式是_____ __ __ |
| (2)取(1)试管中的上层清液滴加酚酞试液。 | 溶液变红色 | 说明原固体中一定含有 。 |
【实验结论】该兴趣小组的同学得出的结论是:氢氧化钠固体 (填“部分变质”
或“全部变质”)。
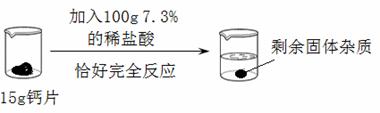
【定量实验】探究氢氧化钠固体的变质程度

请计算,该 氢氧化钠固体的变质程度是___________(精确到0.1%)
氢氧化钠固体的变质程度是___________(精确到0.1%)
下表是NaCl和KCl的溶解度数据,请回答下列问题。
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 (g) | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.2 |
| KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 |
(1)40℃时,氯化钠的溶解度是 g。
(2)将80℃时, 同质量的NaCl和KCl的饱和溶液,分别冷却到0℃,析出晶体最多的是_ (填“NaCl”或“KCl”)溶液。
(3)20℃时,向两只分别盛有35 g NaCl和KCl固体的烧杯中,各加入100g水,充分溶解后,能形成饱和溶液的物质是 ,其溶液的溶质质量分数是______(精确到0.1%)。
(4)温度不变的情况下,若要将接近饱和的KCl溶液变成饱和溶液,可采用的方法是_______________。(写一种)
 Ⅱ.(6分)阅读下列三段材料,回答问题:
Ⅱ.(6分)阅读下列三段材料,回答问题:
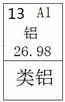
材料一:l869年,俄国化学家门捷列夫对已发现的元素进行研究,制作了元素周期表(右表是其片断),并在他的元素周期表中留下了许多空位代表尚未发现的新元素,其中就预言了“类铝”这种新元素。
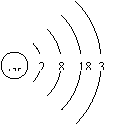 材料二:l875年,法国化学家布瓦博德朗公布了他发现的新元素镓(元素符号为Ga)的性质:镓是银白色金属,密度4.7g·cm-3,能与水剧烈反应生成氢气和氢氧化镓。不久,他收到门捷列夫的来信称:镓就是我预言的“类铝”,其密度应在5.9-6.0 g·cm-3之间。
材料二:l875年,法国化学家布瓦博德朗公布了他发现的新元素镓(元素符号为Ga)的性质:镓是银白色金属,密度4.7g·cm-3,能与水剧烈反应生成氢气和氢氧化镓。不久,他收到门捷列夫的来信称:镓就是我预言的“类铝”,其密度应在5.9-6.0 g·cm-3之间。
材料三:l876年,布瓦博德朗将金属镓提纯后测得镓的密度为
5.94g·cm-3,从而验证了元素周期表的正确性。随后科学家根据元素
周期表的空位,按图索骥,发现了许多新元素。目前金属镓广泛用于
制造半导体材料。镓的原子结构示意图如右图所示。
(1)镓元素的质子数为__________,其氯化物的化学式为_____________。
(2)请根据上述材料,小结金属镓的有关知识:
① 物理性质:镓是银白色金属,密度为5.94g·cm -3
-3
② 化学性质(请用化学方程式表示):_____________________________________;
③ 用途:____________________________________。
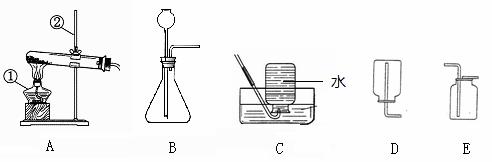
 。该套装置还可用于制取的气体是 ,写出检验该气体的方法____________ ___________ 。
。该套装置还可用于制取的气体是 ,写出检验该气体的方法____________ ___________ 。