|
(NH4)2SO4+2NaOH===Na2SO4+2H2O+2NH3↑; 2NH3+H2SO4 == (NH4)2SO4 。
请计算:
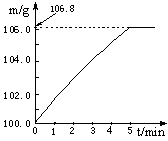
(1)完全反应后产生氨气 g。
(2)该化肥的含氮量为 (精确到0.1%),则这种化肥属于 (填:“合格”或“不合格”。合格硫酸铵含氮量为20%以上)产品。
(3)请计算废硫酸中硫酸的质量分数(写出计算过程)。
(4)若实验过程中氨气被完全吸收,但该实验测得硫酸铵化肥的含氮量高于实际值,其原因是 。
 |
二十一世纪是海洋开发与利用的世纪。以下是某研究性学习小组在探究海水综合利用中遇到的问题,请你参与解决并填空:
问题一、粗盐纯化过程中如何除去可溶性杂质?
粗盐中含有硫酸钠、氯化钙等杂质。提纯时,先向粗盐水中加过量的氢氧化钡溶液,目的是完全除尽______________;再加过量的___________溶液,除去杂质阳离子;滤去沉淀,向滤液中加入______________,除去溶液中的将溶液的_____________________________,调节pH=7,即得到精盐水,再通过蒸发、结晶等过程制得精盐。
问题二、海水“制碱” 的产物成分是什么?
同学们从某企业取回少量碳酸氢钠受热完全分解后的固体样品,为确定其成分,进行了如下探究:
【提出猜想】
甲的猜想:样品中只含有碳酸钠;
乙的猜想:样品中含有碳酸钠和氢氧化钠;
丙的猜想:样品中只含有氢氧化钠。
他们做出上述三种猜想的科学依据是_______________________________________。
【实验、记录与分析】
| 步骤 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量样品于试管中,加水完全 溶解,再加入________________ | ______________________________ | 丙的猜想 不成立 |
| 2 | 取步骤1反应后的溶液于试管中 ___________________________ | ______________________________ | 只有甲的 猜想成立 |
【实验反思】 同学们经过讨论后认为,要验证问题二提出的猜想,下列物质
①HCl溶液、 ②Ca(NO3)2溶液、 ③Ca(OH)2溶液、 ④CuCl2
不能代替步骤1加的试剂的是 (填序号)。
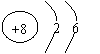 ①3个硫原子 ;
①3个硫原子 ;

