在中学所学的化学反应中,有很多反应没有明显现象.某探究小组想通过实验来证明某些无现象的反应确实发生了,他们做了以下探究过程.
Ⅰ,对NaOH溶液与盐酸反应的探究
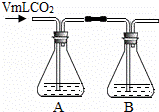
甲同学按如图所示的装置验证NaOH与盐酸发生反应,结果甲同学没有看到预期的实验现象,原因是 ,如果要想证明盐酸与NaOH发生反应,则实验应改为 ,且看到 现象.
Ⅱ,对CO2与NaOH溶液反应的探究
【查阅资料】通常状况下,1体积水能溶解1体积二氧化碳.
【设计实验】甲同学设计了三个实验进行验证,请你帮他完成下列实验报告.
| 实验操作 | 实验现象 | 实验结论及解释 |
|
| ① |
| 氢氧化钠溶液可以与CO2反应. 反应的化学方程式为: | |
| ② |
|
| 氢氧化钠溶液可以与CO2反应. |
| ③ |
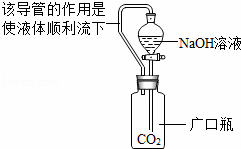
洗气瓶中的溶液均为氢氧化钠溶液或澄清石灰水(均为200mL) | A,B均无明显变化 | 氢氧化钠溶液可以与CO2反应. B中盛放的溶液是 澄 . |
【反思交流】
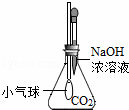
(1)实验①由于甲同学选用的仪器不当,导致未能观察到明显现象,乙同学将甲同学的广口瓶替换成 ,看到了 现象,证明CO2可以与NaOH溶液反应.丙同学认为乙同学的改进实验仍然存在缺陷,应增加一个对比实验,证明CO2确实可以与NaOH溶液发生反应,该对比实验所用的试剂是 .
(2)请判断③中V 200mL(填“>”、“<”或“=”),理由是 .
【实验结论】通过实验探究,证明了氢氧化钠溶液可以与二氧化碳反应.
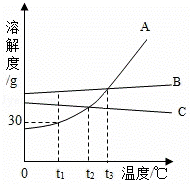
如图为A,B,C三种不含结晶水的固体物质溶解度曲线.下列说法不正确的是( )
|
| A. | t1℃时,65gA的饱和溶液中含有溶质15g |
|
| B. | 要从B的溶液中得到B,通常可采用蒸发溶剂的方法 |
|
| C. | 除去A中含有少量的B,可采用冷却热饱和溶液的方法 |
|
| D. | 在t2℃时,将A,C两种物质的饱和溶液升温到t3℃后,两种溶液中溶质的质量分数仍相等 |
同学们探究金属A,B,C,D的活动性强弱,设计了如下的实验方案:将A放入到B的盐溶液中,无明显现象;将形状和大小相同的A,B和C分别放入相同浓度的稀盐酸中,A表面无明显现象,C产生气泡的速率比B产生气泡的速率慢;将D放入到B的盐溶液中,D表面有固体析出.则金属A,B,C,D活动性由强到弱的顺序为( )
|
| A. | A>B>C>D | B. | D>C>B>A | C. | D>B>C>A | D. | B>C>D>A |
下列说法正确的是( )
|
| A. | 原子是最小的粒子 |
|
| B. | 金刚石、石墨、C60的物理性质存在很大差异的原因是构成它们的碳原子排列方式不同 |
|
| C. | 核外电子排布相同的粒子一定属于同种元素的原子 |
|
| D. | 有一种元素组成的物质一定是纯净物 |
下列分离或提纯物质的方法,所依据的原理正确的是( )
| 选项 | 混合物的分离或提纯 | 分离物质的原理 |
| A | 除去粗盐中的泥沙 | 氯化钠和泥沙的溶解性不同 |
| B | 将石油分馏得到石油产品 | 石油中各成分的密度不同 |
| C | 分离硝酸钾和氯化钠组成的混合物 | 硝酸钾和氯化钠分解温度不同 |
| D | 分离液态空气制取氧气 | 利用氮气和氧气的熔点不同 |
|
| A. | A | B. | B | C. | C | D. | D |
下表是常见的几种酸、碱、盐在水溶液中解离出来离子的情况,根据表中信息分析,得出的结论正确的是( )
| 溶液 | 酸 | 盐 | 碱 |
| |||
| HCl | H2SO4 | NaCl | NaHSO4 | NH4Cl | NaOH | NH3•H2O | |
| 解离出来的离子 | H+,Cl﹣ | H+, | Na+,Cl﹣ | Na+,H+, |
| Na+,OH﹣ |
|
|
| A. | 在水溶液中能解离出H+的物质一定是酸 |
|
| B. | 在水溶液中解离出金属阳离子和酸根离子的物质一定是盐 |
|
| C. | 碱溶液中一定存在金属阳离子和OH﹣ |
|
| D. | 盐溶液中一定存在金属阳离子和酸根离子 |
有100g10%的盐酸溶液,要使其溶质质量分数增大一倍,应采取的方法是( )
|
| A. | 把溶液的量倒掉一半 |
|
| B. | 溶质的质量增大一倍 |
|
| C. | 将100g10%的盐酸与200g25%的盐酸混合 |
|
| D. | 蒸发掉溶剂的质量是原溶液质量的一半 |



 ,Cl﹣
,Cl﹣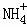 ,OH﹣
,OH﹣